Biotransformace
(přesměrováno z Biotransformace léčiv)
Biotransformace je přeměna chemické struktury látky působením živého organismu. Je katalyzována pomocí enzymů. Biologická aktivita dané látky může být biotransformací snížena, nezměněna nebo zvýšena. Zvýšení biologické aktivity může být terapeuticky pozitivní, pak hovoříme o aktivaci prolátky (prolék, prodrug), i negativní, např. vznik toxického metabolitu.
Vliv polarity a ionizovatelnosti látek[upravit | editovat zdroj]
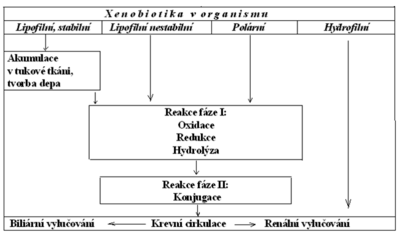
- Hydrofilní, polární či ionizovatelné látky jsou z velké části vylučovány ledvinami v původní formě.
- Lipofilní noxy podléhají extenzivnímu metabolismu:
- jsou reabsorbovány z glomerulárního filtrátu ledvin do krve a transformovány na polárnější metabolity, aby tyto mohly být vyloučeny močí,
- lipofilní látky snadno podléhají enterohepatálnímu metabolismu a částečně se vylučují stolicí.
Biotransformační reakce a jejich klasifikace[upravit | editovat zdroj]
Obvykle se biotransformační reakce dělí do dvou fází, podle osobních preferencí autora té které publikace různě pojmenovávaných. Jednou z možností je dělení na fázi nesyntetickou a fázi syntetickou, které dostatečně a názorně vystihuje rozdíly mezi těmito skupinami biotransformačních reakcí. Alternativně lze hovořit též o první a druhé fázi biotransformace, ale problémem tohoto dělení je fakt, že ne každá látka podléhající biotransformaci prochází oběma fázemi.
Reakce I. fáze, nesyntetické[upravit | editovat zdroj]
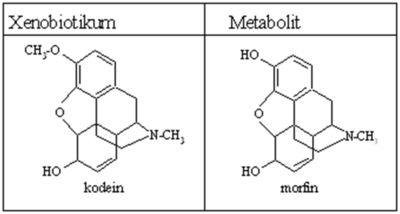
Reakce I. fáze jsou reakce oxidační, v menší míře reakce redukční a hydrolytické. Během nesyntetické fáze dochází ke změnám v molekule transformované látky. Obvykle dochází ke vzniku funkčních skupin umožňujících následné zvýšení hydrofilnosti v syntetické fázi biotransformace. Biologická aktivita látky je obvykle snížena, ale může být i zvýšena (např. enalapril se aktivuje na enalaprilát, kodein se mění na morfin) nebo nezměněna (diazepam se mění na nordiazepam). V této fázi mohou vznikat i toxické metabolity (např. metabolity halotanu, paracetamolu, cyklofosfamidu). Nejčastěji probíhají oxidace, méně často redukce nebo hydrolytické reakce.
Přehled enzymatických systémů podílejících se na nesyntetické fázi:
- oxidační systém rodiny cytochromu P450,
- značí se CYP (rodina)(podrodina)(izoenzym), např. CYP 3A4; popisuje se 17 rodin,
- většina léčiv je metabolizována systémy CYP 3A4 a CYP 2D6,
- mikrozomální oxidační systém,
- mitochondriální aminooxidázy,
- cytoplazmatická alkohol- a aldehyddehydrogenáza,
- xantinoxidáza,
- peroxidázy,
- reduktázy (endoplazmatické retikulum i cytoplazma),
- hydrolázy (např. plazmatické esterázy).
Reakce II. fáze, syntetické[upravit | editovat zdroj]
V této fázi biotransformace vznikají zpravidla neaktivní hydrofilní sloučeniny, které mohou být bez obtíží vyloučeny močí. Podstatou této fáze je připojení hydrofilní funkční skupiny k původní látce. Podle charakteru látky a zejména atakované skupiny může proběhnout několik reakcí:
- glukuronidace – konjugace ‑COOH nebo ‑OH skupiny s kyselinou glukuronovou,
- acetylace – izoniazid, sulfonamidy, anilinové deriváty,
- polymorfismus v acetyláze činí problematickou léčbu tuberkulózy izoniazidem
- konjugace s glycinem – kys. acetylsalicylová, kys. nikotinová,
- konjugace s glutathionem – epoxidy, nitrosloučeniny, kys. etakrynová,
- tvorba éterických sulfátů – minoritní dráha fenolických sloučenin.
Indukce enzymatické aktivity[upravit | editovat zdroj]
Zvýšení aktivity biotransformačních enzymů, působením xenobiotika. Slouží jako ochrana organismu před chemickým stresem. Závisí na dávce induktoru. Indukovat lze zejména CYP oxidázy, tento jev může být podkladem farmakologické tolerance.
Fenobarbitalový typ indukce Zvyšuje se zejména aktivita CYP 2B1, 2B2, 3A1, 3A4 a podrodiny 2C. Je zvyšován metabolismus fenobarbitalu (autoindukce) a dalších látek (heteroindukce), např. tolbutamidu, kortizolu a kumarinu. Obvykle stoupá i hmota jater.
Benzpyrenový typ indukce Zvyšuje se aktivita CYP 1A1, 1A2, glutathiontransferázy, ALA‑syntázy a jiných enzymů. Kromě benzpyrenu se zvyšuje i metabolismus např. 3-metylcholanterenu. Hmota jater stoupá jen nepatrně.
Neindukovatelné enzymy Některé enzymy nelze indukovat. Patří mezi ně např. CYP 2D6.
Inhibice enzymové aktivity[upravit | editovat zdroj]
Snížení aktivity biotransformačních enzymů v důsledku jejich interakce s xenobiotikem. může dojít až k jejich úplné deaktivaci. Projevy intoxikace se mohou objevit již několik hodin po podání látky. Kompetitivně inhibují např. fluorochinolony CYP 3A4, chinidin heteroblokuje CYP 2D6 a cimetidin a ketokonazol mohou blokovat více enzymů ireverzibilní vazbou na hemové železo. Někdy se blokády enzymů i využívá, např. blokáda xantinoxidázy allopurinolem v terapii dny nebo blokáda aldehyddehydrogenázy disulfiramem jako součást terapie závislosti na alkoholu.
Klasifikace enzymů podle IUBMB (International Union of Biochemistry and Molecular Biology)[upravit | editovat zdroj]
Biotransformační reakce xenobiotik jsou katalyzovány různými enzymy. Nejdůležitější je oxidace na enzymatickém systému P45O. Jsou popsány stovky různých enzymů v různých živočišných i rostlinných druzích.
| Hlavní skupina enzymů | Oxidoreduktázy | Hydrolázy | Isomerázy | Transferázy | Lyázy | Lygázy |
|---|---|---|---|---|---|---|
| Podskupiny | Dehydrogenázy Oxidázy Reduktázy Peroxidázy Katalázy Oxygenázy Hydroxylázy |
Esterázy Glykosydázy Peptidázy Thiolázy Fasfatázy Amidázy Daminázy Ribonukleázy |
Racemázy Epimerázy Isomerázy Mutázy |
Acetyl- Methyl- Sulfo- Fosforyl- Transketolázy Transaldolázy |
Dekarboxylázy Aldolázy Hydratázy Dehydratázy Syntházy Lyázy |
Synthetázy Karboxylázy |
Enzymatická katalýza biotransformací I. fáze[upravit | editovat zdroj]
- Nejdůležitější enzymy katalyzující reakce 1. fáze představují hemoproteiny vykazující charakteristické maximum při 450 nm – cytochrom P450 – odpovídá za oxidaci asi 75 % léčiv.
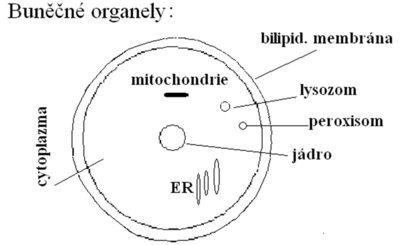
- Cytochrom P450, smíšený enzymový systém oxidázový, je lokalizován na membránách endoplazmatického retikula, mitochondrií či jádra, tj, na membránách mikrosomů – mikrozomální enzymy. Existují jako izoenzymy s různou sekvencí aminokyselin a s rozdílnou substrátovou specificitou.
- volně rozpustné enzymy – lysoenzymy
- tři hlavní genetické rodiny metabolizující léčiva v játrech jsou: CYP 1, CYP 2, CYP 3
- desítky izoenzymů P450: např. CYP1A1, CYP1A2, CYP2C9…
- specificita metabolismu – důležité subtypy P450 a příklady substrátů
| P450 | Převažující lokalizace | Příklady substrátů |
|---|---|---|
| CYP1AB | játra | kofein, theofylin, paracetamol |
| CYP2C9 | játra | ibuprofen, warfarin |
| CYP2C19 | játra | diazepam |
| CYP2D6 | játra, mozek, plíce | kodein, tricyklická antidepresiva |
| CYP2E1 | játra, plíce, CNS, srdce, kostní dřeň | alkohol |
| CYP3A4 | játra, GI, ledviny, plíce, CNS, lymfocyty | erythromycin, nifedipin |
- některá xenobiotika vyvolávají zvýšenou enzymatickou aktivitu – indukci
- jiná xenobiotika naopak enzymatickou aktivitu tlumí – inhibují. např. chronický abuzus ethanolu vede k indukci CYP2E1 – rychlejší metabolismus léčiv
- P450 a biologická variabilita u živočichů – význam výběru experimentálních zvířat pro testování toxicity nových léčiv pro humánní užití.
- interindividuální variabilita uvnitř druhu – genetický polymorfismus enzymů – rychlí a pomalí metabolizátoři – potenciální vznik nežádoucích účinků
- proměnlivost množství enzymu ve tkáních v průběhu života jedince
- některé biotransformační reakce jsou na systému P450 nezávislé
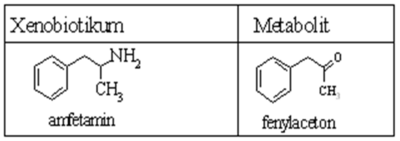
- oxidativní deaminace řady nox (amfetamin) vyžaduje monoaminooxidázy (MAO); nachází se uvnitř buněk vázané na povrch mitochondrií, v ER, v nervových zakončeních, v játrech, ve střevním epitelu
- ethanol je metabolizován rozpustným cytoplazmatickým enzymem alkoholdehydrogenázou vedle mikrosomální oxidázy CYP2E1
- plazmatické esterázy způsobují hydrolýzu nox, jako jsou např. prokain či kokain. Nacházejí se v cytoplazmě v mnohých tkáních, v mikroflóře GI traktu.
| cytochrom P450 závislé procesy | Cytochrom P450 nezávislé procesy |
|---|---|
| alifatická hydroxylace | oxidace primárních, sekundárních,terciárních aminů |
| aromatická hydroxylace | oxidativní deaminace, desulfurace |
| epoxidace dvojné vazby | dehydrogenace (alkohol) |
| N. O. S. – dealkylace | redukce azo, nitro, karbonylsloučenin |
| N. S. P. – oxidace | hydrolýza amidů, esterů |
| deaminace |
Biotransformační reakce II. fáze[upravit | editovat zdroj]
- reakce II. fáze – syntetické, konjugace nox či metabolitů s endogenními substráty – produkce velmi polárních metabolitů, schopných eliminace
- endogenní substráty : glycin, glutathion, kyselina glukuronová, kyselina octová, kyselina sírová
- konjugační enzymy:
- glukuronidace – glukuronosyltransferáza (glukuronyltransferáza) – enzym lokalizován v ER v blízkosti systému cytochromu P450
- sulfatace – sulfotransferáza
- glutathion-S-transferáza
- N-acetyltransferáza (cytozolový enzym v různých tkáních)
- methyltransferázy – přenos methylu z S-adenosylmethioninu na vhodný substrát
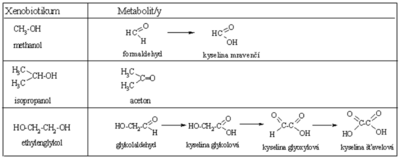
Oxidace alkoholů[upravit | editovat zdroj]
Ethylalkohol[upravit | editovat zdroj]
- hydrofilní látka, snadné vstřebávání (žaludek, střevo)
- rozpustnost v tucích – narkotické účinky
- individuální projevy (muži, ženy), abstinenti – chroničtí alkoholici – adaptace CNS, tolerance
- chronická toxicita – postižení CNS, srdce, játra, ledviny – poškození hepatocytů, zpomalená eliminace
- endogenní tvorba bakteriální fermentací potravy ve střevě (tisíciny promile)
- postmortální vznik alkoholu, hnilobné procesy
Kinetika: rychlost vstřebávání > rychlost eliminace Eliminace kinetika 0. řádu, lineární kinetika
Metabolismus[upravit | editovat zdroj]
- 2–10 % vstřebané dávky se vyloučí dechem a močí, většina se oxiduje v játrech – enzymy ADH (60–70 %), MEOS
Oxidace nenasycených vazeb[upravit | editovat zdroj]
O-Dealkylace[upravit | editovat zdroj]
N-Dealkylace[upravit | editovat zdroj]
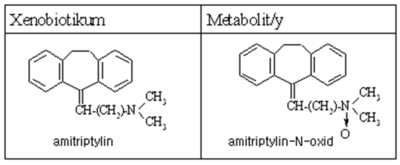
N-Oxidace[upravit | editovat zdroj]
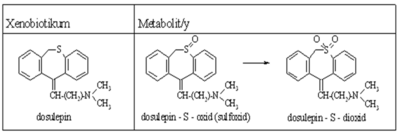
S-Oxidace[upravit | editovat zdroj]
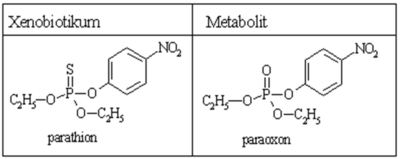
Oxidační desulfurace[upravit | editovat zdroj]
Oxidační deaminace[upravit | editovat zdroj]
Redukce aldehydů a ketonů[upravit | editovat zdroj]
Redukce nitroskupin[upravit | editovat zdroj]
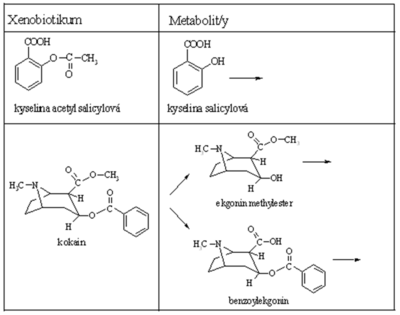
Hydrolýza esterů[upravit | editovat zdroj]
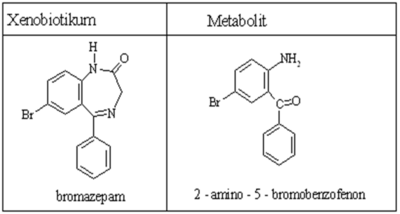
Hydrolytické štěpení cyklů[upravit | editovat zdroj]
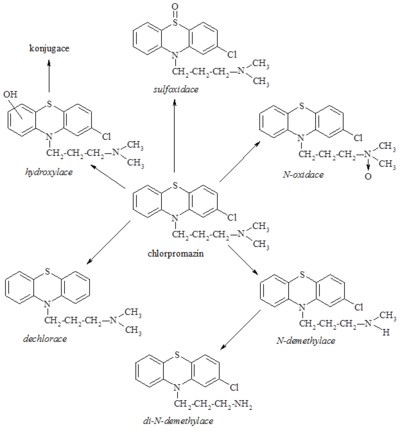
Schéma biotransformace chlorpromazinu[upravit | editovat zdroj]
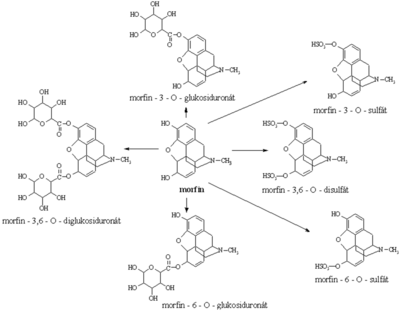
Konjugace morfinu[upravit | editovat zdroj]
Biotransformace heroinu, kodeinu[upravit | editovat zdroj]
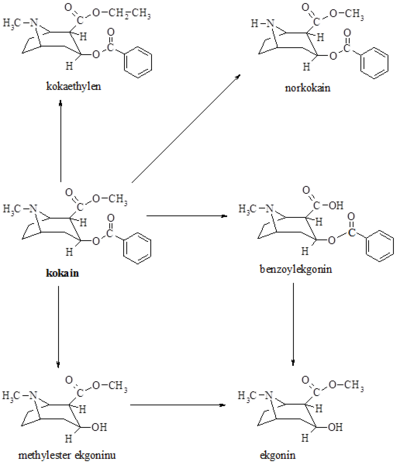
Biotransformace kokainu[upravit | editovat zdroj]
Biotransformace methamfetaminu[upravit | editovat zdroj]
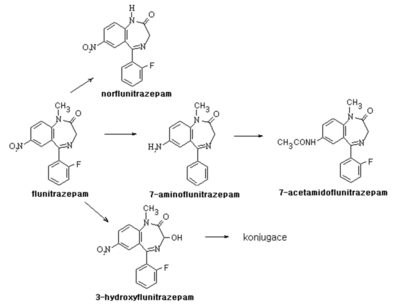
Biotransformace benzodiazepinů[upravit | editovat zdroj]
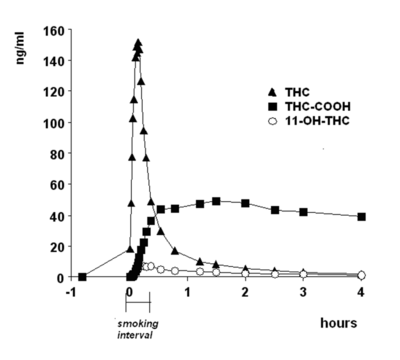
Biotransformace delta-9-THC[upravit | editovat zdroj]
Kinetické aspekty biotransformace[upravit | editovat zdroj]
Znalosti o biotransformaci[upravit | editovat zdroj]
- vývoj a optimalizace toxikologické metody
- interpretace toxikologických nálezů
- poznání mechanismu působení xenobiotik pro účinnou léčbu chorob a intoxikací, omezení nežádoucích účinků léčiv
- farmakokinetika i dynamika: individuální odchylky (genetický základ, zdravotní stav, věk, pohlaví)
- účinky ovlivňuje dávka, frekvence dávek, způsob aplikace, kombinace nox (inhibice či indukce enzymů) aj.
- neočekávané projevy – šokové, komatózní stavy
- posouzení toxikologických nálezů, interpretace – komplexní hledisko s ohledem na okolnosti případu
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Zdroj[upravit | editovat zdroj]
- BALÍKOVÁ, Marie. Osud xenobiotik a biotransformace [online]. [cit. 2012-03-13]. <https://el.lf1.cuni.cz/p88978866/>.
- EYBL, Vladislav. Vybrané kapitoly z obecné farmakologie. Část 1. 1. vydání. Praha : Karolinum, 2003. 63 s. ISBN 80-246-0679-8.