Průtoková cytometrie
Průtoková cytometrie (flow cytometry (FC); flow+cyto+metry~měření buněk v toku) je analytická laboratorní technika používaná k měření fyzikálních a chemických charakteristik jednotlivých částic, často buněk.
Vzorek obsahující buňky nebo částice je suspendován v tekutině a vstřikován do průtokového cytometru. Tenký proud tekutiny unáší vzorek (ideálně po jednotlivých částicích/buňkách) do místa, kam je soustředěn paprsek laseru. Při interakci s buňkami dochází k absorpci, fluorescenci a rozptylu světla. Parametry prošlého, vyzářeného a rozptýleného světla jsou charakteristické pro různé buňky a jejich součásti. Lze tak rychle prozkoumat desítky tisíc buněk a získaná data zpracovat počítačem. Někdy proto bývá průtokový cytometr přirovnáván k "automatickému mikroskopu"[1].
Průtoková cytometrie je využívána v biomedicínském výzkumu, klinické diagnostice a výzkumu buněk. Její výhodou je, že umožňuje kvantitativní analýzu vlastností na úrovni buňky provádět na vzorku s velkým počtem buněk v krátkém čase. Použití této metody umožňuje [2]:
- Počítání buněk
- Třídění buněk
- Stanovení vlastností a funkce buněk
- Detekce mikroorganismů
- Detekce biomarkerů
- Detekce produktů proteinového inženýrství
- Diagnostika zdravotních poruch
- Měření velikosti genomu
Výše zmíněné třídění buněk (FACS Fluorescent Activated Cell Sorting) je specializovaný typ průtokové cytometrie. Poskytuje způsob pro třídění (sorting) jednotlivých buněk heterogenní směsi biologických buněk do dvou nebo více nádob, na základě specifického rozptylu světla a fluorescenčních vlastností každé buňky.
Hlavní části průtokového cytometru[upravit | editovat zdroj]
Průtokový cytometr se skládá ze tří hlavních částí: fluidiky, optiky a elektroniky.
Fluidika[upravit | editovat zdroj]
Pro analýzu je nezbytné, aby se buňky nacházely ve formě suspenze (je totiž nutné, aby částice procházely systémem jedna za druhou a aby procházely konstantní rychlostí). Vzorky krevních nebo kultivovaných buněk se snadno rozptýlí v příslušném roztoku, ale je možné vytvořit buněčné suspenze i z fixovaných a zalitých tkáňových vzorků. Přestože byl průtokový cytometr původně sestrojen k analýze buněk, lze ho dnes použít pro analýzu i menších partikulí (myšleno suspenze těchto částic), například virů a chromozomů. Problémem ale může být nedostatek buněk. Analyzovaná suspenze by měla obsahovat nejlépe 105–106 částic v jednom mililitru. Optimální průměr částic by měl být 1–30 µm. [3]
[4]
Suspenze označených buněk se dávkuje do zkumavky. Ze zkumavky vychází na dolním konci kapilára. Zkumavka je uložena v nádobce s plášťovou tekutinou, která odtéká laminárním prouděním a strhává s sebou z kapiláry jednotlivé buňky. Aby prošla měřícím bodem právě jedna částice, je zajištěno hydrodynamickou fokusací. V případě velkého rozdílu tlaku mezi vzorkem a unášející tekutinou (při vysokém tlaku vzorku), například při rozdílu tlaku 5,5 kPa, je proud vzorku široký, v plošném průřezu tedy proteče více buněk. Při velkém rozdílu tlaku je rozlišení horší. V případě malého rozdílu tlaku mezi vzorkem a unášející tekutinou (při nízkém tlaku vzorku), například při rozdílu tlaku 1,3 kPa, je proud vzorku úzký, a proto v plošném průřezu projde jen jednotlivá buňka. Tento způsob poskytuje lepší rozlišení. Malý rozdíl tlaků je například vhodný pro analýzu DNA.
Dále je nutné zajistit, aby proudění bylo laminární a nikoliv turbulentní. Jestli je proudění laminární nebo turbulentní, je možné stanovit podle Reynoldsova čísla Re. Kritická hodnota Reynoldsova čísla Re je právě hranice mezi laminárním a turbulentním prouděním. Tato hodnota je přímo úměrná průměru trubice d, hustotě tekutiny ρ a střední rychlosti proudu v a nepřímo úměrná viskozitě tekutiny η. [5]
Značení fluorochromy[upravit | editovat zdroj]
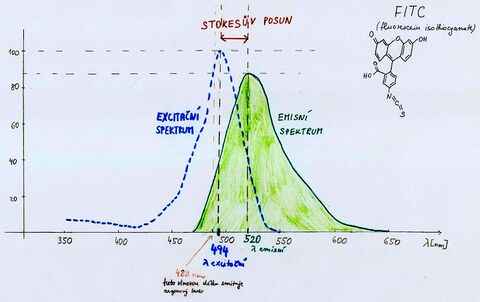
V analyzovaných buňkách se vhodnou metodou znázorní detekovaná látka (například produkt buněčné syntézy imunohistochemicky, DNA Feulgenovou reakcí) tak, aby ji mohl rozpoznat detekční systém přístroje. Některé buňky jsou sice schopny vnitřní fluorescence díky přítomnosti vnitřních fluoroforů (například cytochrom, peroxidáza, hemoglobin), ale ve většině případů se užívá velmi specifických fluorochromů. U fluorochromů je vhodné, aby se jejich absorpční maximum co nejvíce blížilo vlnovým délkám běžně používaných laserů (přehled absorpčních a emisních spekter fluorochromů viz [1]). Tato souvislost vysvětluje, proč je pro mnoho fluorochromů excitační vlnová délka λ= 488 nm (nebo vlnová délka jí velmi blízká) a proč se zároveň používá argonový laser, který emituje záření vlnové délky λ= 488 nm. Pro každý fluorochrom je definován Stokesův posun. Stokesův posun je rozdíl mezi excitační vlnovou délkou a emisní vlnovou délkou (emisní záření má menší energii, tedy menší frekvenci, tedy větší vlnovou délku než excitační záření). Příklad excitačního spektra, emisního spektra a Stokesova posunu u fluorochromu FITC (fluorescein isiothiocyanate) viz vlastnoruční schéma.
V tabulce jsou uvedeny nejčastěji používané flourochromy v průtokové cytometrii. [6]
| zkratka | název | excitační vlnová délka (nm) | emisní vlnová délka (nm) |
|---|---|---|---|
| FITC | Fluoresceinisothiocyanate | 494 | 520 |
| APC | Allophycocyanin | 630 | 661 |
| PE | Phycoerythrin | 488 | 575 |
| PerCP | Peridinin-chlorophyl-protein complex | 488 | 675 |
| PE-Cy5 | Phycoerythrin-Cyanin 5 | 488 | 670 |
| PE-Cy7 | Phycoerythrin-Cyanin 7 | 488 | 774 |
| APC-Cy5.5 | Allophycocyanin-Cyanin 5.5 | 633 | 695 |
| APC-Cy7 | Allophycocyanin-Cyanin 7 | 633 | 785 |
| PE-Texas Red | Phycoerythrin-Texas Red | 488 | 615 |
| PerCP-Cy5.5 | Peridinin-chlorophyl-protein complex-Cyanin 5.5 | 482 | 690 |
| - | AlexaFluor 488 | 495 | 519 |
| - | AlexaFluor 647 | 650 | 668 |
| - | AlexaFluor 594 | 590 | 617 |
| - | AlexaFluor 700 | 696 | 719 |
| - | Pacific Blue | 410 | 455 |
| - | Pacific Orange | 410 | 551 |
| eGFP | Enhanced Green Fluorescent Protein | 498 | 508 |
Optika[upravit | editovat zdroj]
Lasery[upravit | editovat zdroj]
Vzorek je ozářen monochromatickým zářením, nejběžněji jsou používány lasery. Průtokové cytometry bývají dvoulaserové nebo třílaserové. Nejčastěji používaným laserem je vzduchem chlazený argonový laser, který emituje záření s vlnovou délkou 488 nm (modrá oblast spektra), helium-neonový laser s vlnovou délkou 633 nm (červená oblast spektra) a fialový laser s vlnovou délkou 407 nm nebo UV laser s vlnovou délkou 350 nm. [7]
Filtry[upravit | editovat zdroj]
Sběrnou optiku tvoří soustava filtrů, zrcadel a čoček. Zrcadla a filtry rozdělují emitované fotony podle vlnové délky na příslušné detektory (fotony jsou rozděleny do tzv. kanálů). Co se filtrů týče, používají se long pass filtry, short pass filtry, pásmové filtry a dichroické filtry.
Short pass filtry (SP) propouštějí všechny vlnové délky nižší než specifická vlnová délka (např. 600SP propustí všechny kratší vlnové délky než je λ=600 nm).
Long pass filtry (LP) propouštějí všechny vlnové délky vyšší než konkrétní vlnová délka (např. 600LP propustí všechny delší vlnové délky než λ=600 nm).
Pásmové filtry propouštějí specifické rozmezí vlnových délek, Například filtr 575/25BP používaný pro fluorochrom PE (Phycoerythrin) propouští pásmo vlnových délek 562,5 nm až 587,5 nm (tedy 575 ± 12,5 nm; údaj za lomítkem tedy nepředstavuje ± 25 nm, ale rozsah propouštěných vlnových délek celkem, tedy rozdíl mezi nejdelší a nejkratší vlnovou délkou, kterou propustí !!!) a filtr 780/60BP používaný u PE-Cy7 propouští pásmo 750 nm až 810 nm. Použití konkrétních filtrů souvisí s emisní vlnovou délkou každého fluorochromu. Filtr 575/25BP koreluje s emisní vlnovou délkou PE (λemisní =575 nm) a filtr 780/60BP koreluje s emisní vlnovou délkou PE-Cy7 (λemisní =774 nm). Přehled používaných filtrů viz 19. strana odkazu
U diachroických filtrů, které jsou umístěny pod úhlem 45°, část světla projde a část je odražena.
FSC a SSC[upravit | editovat zdroj]
Detektory zaznamenávají:
- přímý rozptyl (forward scatter, FSC)
- boční rozptyl (side scatter, SSC)
- fluorescenci
V případě bočního rozptylu (SSC) a fluorescence je intenzita signálu nízká, a proto je potřeba signál zesilovat fotonásobičem. U přímého rozptylu (FSC) je intenzita dostatečná, není nutno ji zesilovat. Intenzita paprsků FSC je přímo úměrná velikosti buňky, intenzita paprsků SSC odráží vnitřní komplexitu buněk a je úměrná granularitě buňky (stav cytosolu, buněčné inkluze, granula, apod.). Granulocyty a apoptotické buňky mají vyšší hodnoty SSC, které jsou zřejmě způsobené granulací nebo fragmentací jádra. Podle intenzity paprsků FSC je možné rozlišit živé a mrtvé buňky, podle SSC granulózní a agranulózní buňky. [8]
Elektronika (analýza a interpretace získaných dat)[upravit | editovat zdroj]
Signály z optiky jsou převedeny na elektrické impulsy, které jsou zpracovány počítačovým programem.
Při zpracování je třeba:
- odstranit tzv. konfliktní případy (dvě buňky byly měřeny najednou)
- poskládat data naměřená časově odděleně, když se jedná o signál téže buňky
- provést kompenzaci přesvitu fluorochromů (kompenzovat překrývání emisních spekter fluochromů).
Výsledek je pak vyjádřen graficky v podobě buď jednoparametrového histogramu (na ose x je zobrazena intenzita signálu, na ose y četnost) nebo dvouparametrově pomocí dot plotů.
V jednom grafu je tedy možno pozorovat přímý rozptyl (FSC), boční rozptyl (SSC) a fluorescenci (fluorescenční signál poskytují ty částice, které mají navázanou protilátku s fluorochromem). Z grafu se vybere populace buněk (tzv. gatování), která bude předmětem další analýzy, a vytvoří se pro ni dot plot histogram, kde se na obě osy vynesou parametry, které je třeba zkoumat.
[3]
[7]
Ilustrační příklad[upravit | editovat zdroj]
Ilustrační příklad (dále uvedený) se týká obrázku (vlastní rukou provedeného nákresu podle odkazu [2]
, obrázek z deváté stránky prezentace).
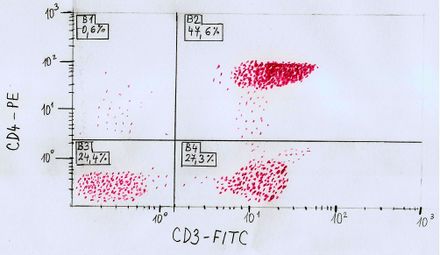
Na osu x se vynáší jeden z parametrů. V tomto případě přítomnost epitopu CD3, respektive fluorochromu FITC (Fluoresceinisothiocyanate), který je navázán na monoklonální protilátku proti CD3 epitopu (antigenu). CD3 epitop (CD=Clusters of Differentiation, tzv. diferenciační znaky, znaky definované struktury rozpoznatelné monoklonální protilátkou, v současné době je na lidských leukocytech charakterizováno a označeno více než 200 protilátek) [9] [10]
je přítomen na povrchu lymfocytů.
Na osu y se vynáší druhý z parametrů. V tomto případě se jedná o epitop CD4, respektive je zde zaznamenáno navázání fluorochromu PE (Phycoerythrin) na monoklonální protilátku proti CD4 epitopu. CD4 epitop se nachází v subpopulaci pomocných lymfocytů.
Graf bývá rozdělen do 4 kvadrantů.
- V 1. kvadrantu jsou buňky pozitivní pouze pro znak vynesený na ose y, tedy v tomto konkrétním případě buňky pozitivní pro antigen CD4 (v tomto ilustračním příkladu se jedná o 0,6 % buněk).
- V 2. kvadrantu jsou buňky pozitivní pro znaky vynesené na obou osách (x,y), tedy buňky tohoto kvadrantu obsahují oba antigeny (CD3 i CD4). V tomto ilustračním příkladu vykazuje pozitivitu obou antigenů přibližně 47,6 %.
- Buňky 3. kvadrantu jsou negativní pro oba sledované znaky. V ilustračním příkladu se v tomto kvadrantu tedy nachází 24,4 % buněk.
- Ve 4. kvadrantu jsou buňky pozitivní pouze pro znak vynesený na ose x, tedy v tomto případě pouze pro antigen CD3. Ve čtvrtém kvadrantu se nachází asi 27,3 % buněk.
Relativní intenzita fluorescence je vynesena na osách v exponenciální stupnici.
Tabulka výskytu epitopů (antigenních determinantů) zkoumaných v průtokové cytometrii [11] [12] [3]
| epitopy | výskyt |
|---|---|
| CD38+ | plazmatické buňky |
| CD14+ | monocyty |
| CD15+ | granulocyty |
| CD3+ | zralé T lymfocyty |
| CD4+ | subpopulace pomocných T lymfocytů |
| CD8+ | subpopulace cytotoxických T lymfocytů |
| CD25+ | aktivované T lymfocyty |
| CD19+, CD5+ | zralé B lymfocyty |
| CD56+, CD16+ | NK buňky |
Typy sorterů[upravit | editovat zdroj]
Podle způsobu práce rozeznáváme dvě základní skupiny sorterů:
- elektrostatický kapénkový sorter (electrostatic droplet sorter)
- fluidní switch sorter (fluidic switch sorter)
Elektrostatický kapénkový sorter[upravit | editovat zdroj]
K vychýlení buněk využívá elektrostatické sily. Buňky jsou vstříknuty do vzduchu v proudu nosné kapaliny, k rozbití souvislého proudu kapaliny na kapénky se využívá vibračních vln. Nabité kapénky jsou vychýleny z hlavního proudu směrem k jedné z nabitých desek, tyto kapénky jsou sbírány, zatímco nenabitý hlavní proud směřuje do odpadní nádrže. Kapénkový sorter má vysokou rychlost separace a vyseparované populace jsou koncentrované.
Fluidní switch sorter[upravit | editovat zdroj]
Fluidní switch sorter umožňuje sortovat i veliké částice a nehrozí u něho biologické riziko, ale dochází u něho k většímu naředění vyseparované populace a také sortovací rychlost je menší než u kapénkového sorteru. Tyto sortery můžou pracovat na různých principech. Při prvním principu proud nosné kapaliny se vzorkem prochází kanálem, při identifikaci částice splňující požadovaná kritéria je sepnut piezoelektrický ventil a proud s částicí vybočí mimo hlavní proud. Při druhém principu je sběrná trubice pro požadovaný vzorek posunuta do středu toku proudu a vysouvá se a zasouvá do proudu kapaliny v případě detekce požadované částice.
Rychlost sortování[upravit | editovat zdroj]
Délka sortu závisí na kvalitě vzorku a typu buněk. Sort buněk malých (např. thymocytů) trvá kratší dobu než sort velkých, křehkých, adherentních buněk. 1 milion makrofágů je za optimálních podmínek vysortován za 3 minuty, 1 milion thymocytů je vysortován asi za 45 sekund. U jednoho průtokového cytometru s vysokorychlostním sortem je například uvedeno, že jeho standardní sortovací rychlost je 6 000 buněk/sekundu a že dokáže ve vysokorychlostním modu vyseparovat až 25 000 buněk za sekundu. [13]
Výhody a nevýhody průtokové cytometrie[upravit | editovat zdroj]
Výhody[upravit | editovat zdroj]
- Přednost této techniky spočívá především ve vysoké frekvenci analýzy jednotlivých částic.
- Velké množství analyzovaného materiálu – velké objemy dat.
- Analýza trvá pouze několik minut a poskytuje velké množství informací.
- Lze provádět jak kvalitativní, tak kvantitativní analýzu.
- Jsou zde možné manipulační operace – např. třídit buňky s vybranými vlastnostmi (cell sorting). Sortování je určeno především pro vědecké účely, v klinické praxi se však moc nevyužívá.
- Jednoduchá příprava vzorku k analýze. (Celá příprava většinou nezabere víc než 1 hodinu.)
Nevýhody[upravit | editovat zdroj]
- Nevýhodou průtokové cytometrie je její vysoká finanční náročnost – limitujícím faktorem pro praktické použití je cena průtokových cytometrů.
- Sestavení experimentu, analýza a vyhodnocování dat závisí na zkušenostech obsluhy.
- Při analýze pevných tkání je nezbytné jednotlivé buňky separovat od sebe. Během této separace však může dojít ke změně či ztrátě vlastností buněk.
Využití průtokové cytometrie v medicíně[upravit | editovat zdroj]
- Výzkum rostlinných, živočišných a lidských buněk.
- Výzkum kvasinek, coby stále významnějšího modelu vyšších eukaryot.
Aplikace průtokové cytometrie zasahují do všech odvětví klinické praxe. Největší uplatnění mají v klinické imunologii, hematoonkologii, nádorové biologii a v oblasti molekulární biologie.
Průtoková cytometrie se většinou používá pro vyšetření:
- KRVE – v absolutním a relativním zastoupení – celkové T lymfocyty, pomocné/induktorové T lymfocyty, tlumivé/cytotoxické T lymfocyty, aktivované T lymfocyty, B lymfocyty, aktivované/nezralé B lymfocyty, NK buňky spontánní cytotoxicity, vyšetření trombocytů – retikulované trombocyty, aktivované trombocyty, trombocytární glykoproteiny, vázané imunoglobuliny na trombocytech; ilustrační příklad žádanky na vyšetření periferní krve průtokovou cytometrií
- KREVNÍ DŘENĚ – podobná indikace jako u vyšetření periferní krve; při odběru použití speciální zkumavky s antikoagulačním roztokem
- LYMFATICKÉ UZLINY – například diagnostika lymfomu, odlišení karcinomu lymfatické uzliny od reaktivní uzliny; odebrání do gázy navlhčené ve fyziologickém roztoku
- LIKVORU (mozkomíšního moku)
- VÝPOTKŮ
- BRONCHOALVEOLÁRNÍ LAVÁŽE (BAL)
Průtoková cytometrie se tedy používá například při odlišení reaktivní a monoklonální lymfocytozy, rozlišení akutní lymfoblastické a myeloidní leukemie, vyloučení či potvrzení paroxysmální noční hemoglobinurie a vlasatobuněčné leukemie HCL při pancytopenii, diagnostice lymfomů, trombocytémie, při diagnostice defektů imunity (například diagnostice a monitorování autoimunitních chorob), v transplantační imunologii a v mnohém dalším. [11]
[14]
[15]
[16]
Průtoková cytometrie je také využívána pro
- analýzu DNA a RNA
- testování aktivace bazofilů na konkrétní alergen nebo skupinu alergenů (alergie na plevel – např. ambrosii, pelyněk; traviny; dřeviny; roztoče, plísně; na zvířata – na psy, na kočky; na hmyz – vosy, včely) [17]
- vyšetření integrity akrozomu – schopnost spermie proniknout do oocytu [18]
- analýze životnosti (zastoupení apoptických buněk)
- měření koncentrace intracelulárního vápníku (k tomuto stanovení lze použít i měření s pomocí fluorescenčního mikroskopu). [19]
Úhrada ze zdravotního pojištění[upravit | editovat zdroj]
Průtoková cytometrie je výkon hrazený zdravotními pojišťovnami. V Seznamu zdravotních výkonů s bodovými hodnotami, který vydalo Ministerstvo zdravotnictví ČR pro rok 2013, je pod kódem výkonu „91439 – Imunofenotypizace buněčných subpopulací dle povrchových znaků – průtoková cytometrie“ a „91475 – Interpretace souboru imunologických laboratorních vyšetření laboratorním pracovníkem – lékařem specialistou v oboru lékařské imunologie písemná“. Výkon 91439 je ohodnocen 319 body a výkon 91475 je ohodnocen 116 body. Oba výkony lze nasmlouvat pouze na specializovaném pracovišti.
Počty vykázaných výkonů[upravit | editovat zdroj]
Za 1. pololetí roku 2013 Všeobecná zdravotní pojišťovna ČR uhradila za své klienty v celé České republice 42 028 výkonů průtokové cytometrie (kód výkonu 91439). [20]
Odkazy[upravit | editovat zdroj]
Externí odkazy[upravit | editovat zdroj]
- Průtoková cytometrie, Zdenka Sedláková, DocPlayer
- Demystifikace optického systému průtokové cytometrie: Nahlédnutí pod pokličku
- Přehled emisních a absorpčních spekter nejpoužívanějších fluorochromů
- Přehled používaných filtrů pro jednotlivé fluorochromy při průtokové cytometrii (19. strana odkazu)
- Zdroj obrázku použitého u ilustračního příkladu (z deváté stránky prezentace)
- Příklad žádanky na vyšetření průtokovou cytometrií
Reference[upravit | editovat zdroj]
- ↑ https://docplayer.cz/34616405-Prutokova-cytometrie.html
- ↑ https://en.wikipedia.org/wiki/Flow_cytometry
- ↑ a b c ROUBALOVÁ, L.. Průtoková cytometrie [online]. [cit. 2013-25-11]. <http://web2.stapro.cz/bullfons/22012/labo1.pdf>.
- ↑ SHAPIRO, Howard M. Practical flow cytometry 4th ed. 4.vydání vydání. John Wiley and sons, 2003. ISBN 978-0-471-41125-3.
- ↑ NAVRÁTIL, Leoš a Jozef ROSINA, et al. Medicínská biofyzika. 1 (dotisk 2013) vydání. Grada Publishing, 2005 (dotisk 2013). 524 s. s. 119 (definice Reynoldsova čísla). ISBN 978-80-247-1152-2.
- ↑ LANGHANSOVÁ, HELENA. Využití průtokové cytometrie v imunologii [online]. České Budějovice : Jihočeská univerzita, 2011, dostupné také z <http://biomedicina.prf.jcu.cz/wordpress/wp-content/uploads/2011/12/Vyuzitiprutokovecytometrievimunologii.pdf>.
- ↑ a b výuková prezentace 2. lékařské fakulty UK v Praze, Průtoková cytometrie, Praha 2009, http://imunologie.lf2.cuni.cz/soubory_vyuka/Prutokova%20cytometrie_Laboratorni%20vysetrovaci%20metody.pdf
- ↑ BERNAND, Vladan. Průtoková cytometrie : flow-cytometrie [online]. Brno : Biofyzikální ústav Lf Masarykovy univerzity, rok neuveden, dostupné také z <http://www.med.muni.cz/biofyz/files/gerontologie/prutokova_cytometrie_prezentace.pdf>.
- ↑ Laboratoř AIDS a infekční imunologie. Princip průtokové cytometrie [online]. [cit. 2013-12-01]. <http://www1.lf1.cuni.cz/~hrozs/flowcyt1.htm>.
- ↑ Oddělení fyziologie a imunologie živočichů PřF Masarykovy univerzity. Práce s buňkami imunitního systému : název souboru bunky_imunity.ppt [online]. Brno : Oddělení fyziologie a imunologie živočichů Přírodovědecké fakulty Masarykovy univerzity, rok neuveden, dostupné také z <http://www.sci.muni.cz/ofiz/index_cz.php?page=studies&sub=materialy>.
- ↑ a b laboratorní vyšetření v klinické imunologii a alergologii. přehled vyšetření -> Stanovení subpopulací lymfocytů periferní krve [online]. [cit. 2013-11-29]. <http://www.interimun.cz/prehled-vysetreni-13-stanoveni-subpopulaci-lymfocytu-periferni-krve.htm/>.
- ↑ Lékařská fakulta UK v Plzni. Průtoková cytometrie (2.c seminar prutokova cytometrie.ppt). Plzeň, rok neuveden,
- ↑ {{Mikrobiologický ústav Akademie věd ČR. FACS Vantage SE [online]. [cit. 2013-12-01]. <http://www.cytometry.cz/sysmenu.php?rstext=odkaz&rstema=17&rslink=sysmenu/VantageCZ.htm&stromhlmenu=9:17>.
- ↑ BRZOVÁ, Petra. Průtoková cytometrie základní princip a klinické využití. Nemocnice s poliklinikou Havířov, rok neuveden,
- ↑ ÚHKT - Ústav hematologie a krevní transfuze. žádanka o vyšetření průtokovou cytometrií [online]. [cit. 2013-11-30]. <http://www.uhkt.cz/zdravotnik/komplement-laboratori/laboratorni-prirucky-zadanky/laborator-prutokove-cytometrie/116_LP_08_01_Priloha1.pdf>.
- ↑ Ústav alergologie a imunologie FN Plzeň. Vyšetření parametrů buněčné imunity : název souboru Stanoveni parametru bunecne imunity.ppt. Plzeň, rok neuveden,
- ↑ imalab. test aktivace bazofilů [online]. [cit. 2013-11-30]. <http://www.imalab.cz/clanek/266-test-aktivace-bazofilu.aspx>.
- ↑ imalab. integrita akrozomu [online]. [cit. 2013-11-30]. <http://www.imalab.cz/clanek/262-integrita-akrozomu.aspx>.
- ↑ ČÍHAL, Martin. METODY MĚŘENÍ KONCENTRACE INTRACELULÁRNÍHO VÁPNÍKU [online]. Brno : Vysoké učení technické v Brně, 2011, dostupné také z <https://dspace.vutbr.cz/bitstream/handle/11012/2001/Bakal%C3%A1%C5%99sk%C3%A1%20pr%C3%A1ce-xcihal04.pdf?sequence=1>.
- ↑ zdroj: Informační systém VZP ČR
Použitá literatura[upravit | editovat zdroj]
- JIRKOVSKÁ, Marie. Histologická technika : Pro studenty lékařství a zdravotnické techniky. 1. (dotisk 1. vydání) vydání. Praha : Galén, 2009. ISBN 978-80-7262-263-4.
- Přírodovědecká fakulta Masarykovy univerzity. Genotoxicita a karcinogeneze - oddíl kontrola hemopoézy a leukemie - pododdíl Diagnostika, léčba, terapeutické využití cytokinů [online]. [cit. 2013-12-01]. <https://is.muni.cz/do/rect/el/estud/prif/ps13/genotox/web/pages/12_kontrola.html>.
- NOVÁK, BASAŘOVÁ, FIALA, DOSTÁLEK, Jan, Gabriela, Jaromír, Pavel. Průtoková cytometrie ve výzkumu kvasinek Saccharomyces cerevisiae a její aplikace v praxi [online]. [cit. 2013-25-11]. <http://www.chemicke-listy.cz/docs/full/2008_03_183-187.pdf>.
Doporučená literatura[upravit | editovat zdroj]
- PROF. MUDR. ECKSCHLAGER, Tomáš, Csc.. Průtoková cytometrie v klinické praxi. 1.vydání vydání. Praha : Grada Publishing, 1999. ISBN 80-7169-279-4.