Množení bakterií in vitro
Růst a množení bakterií představuje řadu biochemických a fyzikálních procesů.
Růstový cyklus sestává z těchto částí:
- růst buňky – koordinovaná tvorba makromolekul a buněčných složek;
- tvorba septa;
- dělení buňky.
Generační doba je doba mezi dvěma děleními.
Doba zdvojení je doba, za jakou se počet bakterií zdvojnásobí.
Dělení bakterií probíhá za ideálních podmínek geometrickou řadou ve skutečnosti tomu tak není především z těchto důvodů:
- vyčerpání živin (resp. se živiny nedostanou ke všem);
- inhibice zplodinami svého metabolismu.
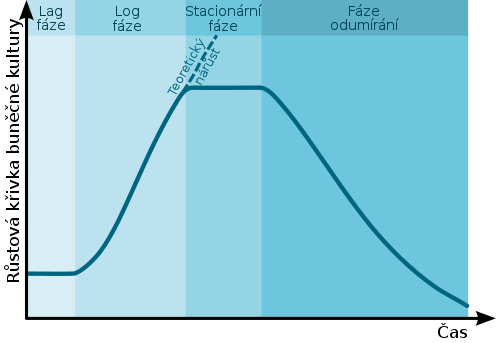
Růstová křivka
Růstová křivka znázorňuje závislost počtu živých buněk (v logaritmické stupnici) na stáří kultury. Na růstové křivce popisujeme následující části:
- lag-fáze – prodleva v dělení na počátku, probíhá syntéza enzymů, zvětšování objemu, délka fáze závisí na stavu inokula (krátká pokud použity buňky z fáze růstu), počátek dělení má nestálou rychlost;
- logaritmická (exponenciální) fáze – konstantní rychlost dělení, závisí na druhu mikroba, teplotě, složení prostředí
- specifická růstová rychlost je růstová rychlost na jednotku biomasy;
- stacionární fáze – buňky už se téměř nedělí, roste množství odpadních produktů, buňky nepřibývají ani neubývají, délka fáze závisí na druhu bakterií a charakteru prostředí
- x = Y × s
- x je koncentrace vytvoření biomasy, s koncentrace spotřebované živiny, Y růstový výtěžek (informuje o fyziologii rostoucí bakterie);
- fáze odumírání (autolýza) (neisserie nebo pneumokoky), indukce enzymů destruujících buněčnou stěnu, porušení rovnováhy mezi lytickým působením a syntézou stěny;
- někdy je rychlost konstantní (jediný nepříznivý faktor), většinou však působí několik faktorů, kinetika je tak různá;
- specifická rychlost hynutí je rychlost úbytku buněk přepočtená na jednu buňku.
Při kontinuální kultivaci dochází k udržení v logaritmické fázi, je potřeba zajistit přívod živin a odvod odpadu. Kontinuální kultivaci provádíme v přístrojích zvaných fermentory, využívá se například k produkci ATB, přirozeně probíhá v GIT.
V přirozených podmínkách se bakterie množí většinou pomaleji v důsledku omezeného přívodu, suboptimální teploty a působení ostatních mikrobů.
V praxi se růst bakterií sleduje měřením nárůstu buněčné hmoty, a to následujícími způsoby:
- spektrofotometricky;
- počítáním buněk (mikroskopicky v počítací komůrce);
- kultivačně na zúženém kultivačním médiu na Petriho misce.
Biofilm
Biofilm je struktura tvořena bakteriemi, která slouží k jejich adherenci, komunikaci a ochraně. Také může být faktorem patogenity a virulence. Adheruje k povrchům inertním či anorganickým (vlhké povrchy v přírodě, implantáty, katetry, kanyly) i živým (epiteliální buňky). Je to složitá struktura s kanálky (voda přináší živiny a odnáší odpad). Připomíná tkáně vyšších organismů. Na jeho vzniku se většinou podílí několik druhů mikrobů.
Biofilm zvyšuje odolnost bakterií (před nepříznivými podmínkami prostředí nebo imunitními mechanismy) a umožňuje jejich bohatou komunikaci, což může značně komplikovat léčbu.
Vznik biofilmu
Přilnutí (adheze) bakterií na povrch (pomocí fimbrií, glykokalyxu, povrchových proteinů atd.) podmíní spuštění genů pro tvorbu extracelulárních polymerů. Další buňky vznikají v extracelulární polysacharidové hmotě. Dělením vzniknou tzv. mikrokolonie, které rychle rostou. Mikrokolonie se obalí slizem a diferencuje v biofilm. Mohou být tvořeny nejen bakteriemi, ale také vyššími organismy (v těle např. Candida albicans). Z biofilmu se mohou uvolnit volné buňky (planktonické buňky) a kolonizovat jiná místa.
Komunikace bakterií prostřednictvím biofilmu spočívá především ve výměně genetické informace (např. plazmidů) mezi bakteriemi. Tím mohou bakterie získat například rezistenci vůči antibiotikům.
- Quorum sensing
- Mechanismy, kterými mohou bakterie vnímat přítomnost jiných bakterií ve svém okolí a přizpůsobovat se jim. Bakterie při svém růstu produkují tzv. autoinduktory. V momentě, kdy koncentrace autoinduktorů dosáhne prahové koncentrace, dojde k ovlivnění transkripce genů množících se bakterií. Touto změnou exprese genů mohou podmínit zastavení růstu bakterií nebo její další růst. Tímto mechanismem si kolonie udržuje optimální hustotu populace.
- Dalším faktorem, který mohou autoinduktory ovlivňovat je produkce některých metabolitů (např. produkce proteáz u Pseudomonas aeruginosa).
Biofilm lze pozorovat konfokálním laserovým mikroskopem v optických řezech a z nich složit prostorovou strukturu. Tloušťka biofilmu kolísá od několika až do stovky mikrometrů, podle dostupnosti živin.
Příklady míst tvorby biofilmu
- Zubní plak – viridující streptokoky.
- Periodontitida – v kapsách pod dásní (tvorba polymikrobiálního biofilmu, kam neproniká kyslík), nahromaděná bakteriální hmota, odumřelé buňky a hnisavé buňky situaci zhoršují.
- Zánět středního ucha – hemofily.
- Osteomyelitis – Staphylococcus aureus;
- Cystická fibróza, k primárním respiračním infekcím se přidávají chronické nebo opakující se infekce. Dochází k ucpávání průdušek a trvalé poškození epitelu. Na tomto poškozeném epitelu se biofilmem usadí Pseudomonas aeruginosa a jí podobné.
- Záněty žlučových cest – G− střevní tyčinky.
- Při chronickém zánětu prostaty – bakterie pronikají do prostaty proti proudu moče, akutní prostatitida může přejít v chronickou. Zpočátku je biofilm jen komplikace, později i příčina onemocnění.
- Špatně vyživovaná kůže a podkoží při bércových vředech, na povrchu popálených ploch.
- Nitroděložní tělísko může být příčinou zánětů v dutině pánve a sepse.
- Asistované dýchání – tvorba na stěně trubic. Při nedostatku ošetřování mohou bakterie proniknout až do průdušek a plic.
- Intravenózní katetry – koaguláza negativní stafylokoky.
- Umělé srdeční chlopně.
- Kloubní náhrady.
- Kontaktní čočky − při nesprávném užívání se usazuje Pseudomonas aeruginosa.
- V urologii je biofilm nejčastější příčinou infekce při zavedeném močovém katétru.
Rezistence buněk biofilmu k antibiotikům
Buňky biofilmu jsou velmi rezistentní k antimikrobním látkám a dezinfekcím (až tisíckrát více než buňky planktonické). V lékařské praxi to znamená, že k léčbě nestačí ani vysoké dávky antibiotik. Odolnost je vyjádřena fenotypově − nejde o rezistenci podmíněnou geneticky.
Laboratorní vyšetření citlivosti vůči antibiotikům podává nesprávné výsledky. Bakterie biofilmu jsou rezistentní, ale oproti planktonickým bakteriím se v optimálních laboratorních podmínkách jeví jako citlivé.
Odolné buňky tolerující antibiotikum a setrvávající v těle se obecně nazývají perzistoři. V biofilmu se mezi buňkami přenáší geny až tisíckrát úspěšněji, než mezi planktonickými buňkami (podpora přenosu genů rezistence v populaci). Hlenovou hmotou jsou buňky v biofilmu také fyzicky chráněny před protilátkami.
Faktory ovlivňující množení bakterií
- kyslík
- aerobní – Pseudomonas, kyslík akceptor elektronů
- fakultativně anaerobní – enterobakterie
- anaerobní – klostridia
- mikroaerofilní – Neisseria
- kapnofilní – meningokoky, gonokoky
- voda
- většina hygrofilní (x lyofilizace – sušení zmražených bakterií ve vakuu), k vyschnutí odolnější G+ a acidorezistentní (stafylokoky a korynebakteria na kůži)
- xerofilní – voda na povrchu částic (půda), nokardie, aktinomycety, plísně
- teplota – minimální, optimální a maximální růstová teplota – teplotní rozmezí
- psychrofily – 0–20 °C
- psychrotolerantní – yersenie, listerie, salmonelly, S. aureus
- mesofily – 20–40 °C
- termofily – nad 40 °C
- hypertermofily – nad 80 °C
- hydrostatický tlak – hlubokomořské
- osmotický tlak – většinou hypotonické prostředí, ochrana stěnou
- hypertonické – plasmolýza (konzervace potravin)
- halofily – halotolerantní a obligátní (enterokoky, stafylokoky, Vibrio) nebo extrémní halofily
- pH
- neutrofily – většina
- alkalofily – Vibrio cholerae, alkalotolerantní – Proteus, enterokoky
- acidofily – laktobacily
- oxidoredukční potenciál
- aeroby – oxidované prostředí
- anaeroby – potřeba nízký potenciál
- záření – poškození ultrafialovým a ionizačním zářením
Odkazy
Související články
Zdroj
- JANSKÝ, Petr. Zpracované otázky z mikrobiologie [online]. [cit. 2012-02-06]. <https://www.yammer.com/wikiskripta.eu/uploaded_files/3804405>.