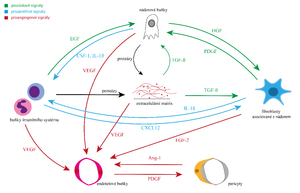
Nádorové mikroprostředí
Z WikiSkript
Složení nádorů[upravit | editovat zdroj]
1. Nádorový parenchym
- vlastní nádorové buňky
- podle nich název nádoru
- diferencovanost (stupeň podobnosti s výchozí tkání)
2. Nádorové stroma
- fibroblasty, buňky imunitního systému, endoteliální buňky (cévy)
- výživa a kostra nádoru
- transportní funkce (přenos signálů, rezervoár a vyplavování růst. faktorů, cytokinů a dalších)
- klíčová úloha při nádorové angiogenezi a metastazování
Poměr mezi parenchymem a stromatem určuje konzistenci nádoru:
- převaha stromatu – nádor tuhý až tvrdý (skirhotický nádor)
- převaha parenchymu – měkký (medulární nádor)
Tvorba nádorového stromatu probíhá paralelně s proliferací nádorových buněk.
- iniciálním pochodem je únik plazminogenu, fibrinogenu a dalších koagulačních faktorů z cév v důsledku zvýšené kapilární permeability (ta je indukována působením faktoru VEGF – vascular permeability factor, uvolňují jej nádorové buňky)
- vzniká tedy extracelulární fibrinový gel, do nějž vcestují fibroblasty, které pod vlivem dalších faktorů proliferují a vytváří stroma nádoru
- proliferace nádorových buněk a růst nádoru jsou vázány na vhodné mikroprostředí (stroma), ale závislost též na schopnosti migrace, průniku do cév a metastazování – zde je klíčová role enzymů souhrnného názvu metaloproteázy (MMP) – početná rodina (kolagenázy, elastázy, gelatinázy a další) a ty vznikají převážně v buňkách stromatu (ve fibroblastech) jako odpověď na přítomnost nádorových buněk
- MMP se významně uplatňují v procesu metastazování a angiogeneze.
Metastazování[upravit | editovat zdroj]
- skryté šíření do oblastí anatomicky vzdálených prvotnímu ložisku
- nádor se může šířit přímo (prorůstá-li do serozních dutin), nádorové buňky se mohou uchytit a proliferovat na povrchu jiných orgánů (implantační metastázy) nebo se šíří dutými orgány (porogenní metastázy)
- většinou jde o vícestupňový proces, probíhající ve 4 metastatických kaskádách a je výsledkem porušené rovnováhy mezi aktivačními a inhibičními faktory
- spouštěcím mechanismem, odpovědným za změnu buněčného fenotypu v metastatický, je pravděpodobně mutace onkogenu ras
Etapy kaskády
- Invaze nádoru do okolí (nutný průnik nádorové buňky bazální membránou a intersticiálním stromatem)
- bazální membrána – obsahuje kolagen typu IV. a specifické glykoproteiny (laminin, fibronektin)
- intersticiální stroma – kolagen typu I. a III., elastin, proteoglykan
- nádorové buňky interagují s bazální membránou pomocí receptorů (receptory pro laminin a hlavně pro integriny) – buňka pomocí receptoru přilne k bazální membráně → vlastní narušení membrány proteolytickými enzymy (uvolňovanými z nádorových buněk) – jde hlavně o metaloproteázy (obsahují hlavně kolagenázy – proteolýza kolagenu IV.), serinproteázy, cysteinproteázy
- po narušení membrány → invaze nádorových buněk mechanicky (při zvýšeném tlaku uvnitř rostoucího nádoru)
- nádorová buňka proniká do mízních a krevních kapilár (klíčový faktor umožnující invazi: E-cadherin)
- Transport nádorových buněk lymfatickou/krevní cestou
- mezi oběma cévními systémy jsou spojení – přítomnost nádorové buňky v uzlině vyvolá imunitní reakci (uzlina se zvětšuje, může se zvětšit i pro nádorovou infiltraci, pokud imunitní systém selhal)
- průnik do cirkulace – nádorové buňky jsou v nepříznivém prostředí (přežije jen zlomek) – buňky jsou eliminovány: nespecifická destrukce (makrofágy, granulocyty), imunologické mechanismy (T-lymfocyty, NK-bb.), mechanické faktory (turbulence krve), tzv. kyslíkový efekt (zvýšená tenze kyslíku v arteriální krvi a v plicních kapilárách) a dále se na destrukci podílí účinek NO (uvolňovaný z aktivovaných makrofágů, má cytotoxický účinek a indukuje apoptózu, na druhé straně usnadňuje přichycení nádorových buněk k endotelu – působí vazodilataci a potencuje agregaci destiček)
- Nidace nádorových buněk a jejich zpětný průnik do tkáně
- nejčastěji v kapilární síti parenchymatozních orgánů
- v cirkulaci tvoří nádorové buňky agregáty s destičkami, agregát se snáze zachytí v kapilárách
- dochází k adhezi destiček (adhezní molekuly: cytoadheziny, E-cadherin) a jejich degranulaci (uvolnění např. tromboxanu A2); působí ireverzibilní agregaci a fixaci trombu s nádorovými buňkami na cévní stěnu
- Průnik uchycených buněk zpět do tkáně (podobně jako první etapa)
- PDGF (růstový faktor z trombocytů) stimuluje mimo jiné proliferaci buněk mikrometastázy a současně uvolněný serotonin může změnou permeability kapilár usnadnit průnik nádorových buněk
- mikroembolus je odolný, (ve srovnání s volnými nádorovými buňkami) neb se obaluje fibrinem (vznikajícím jako produkt plazmatické koagulace), obal chrání buňky proti mechanické traumatizaci a maskuje nádorové buňky před imunokompetentními lymfocyty
Růst metastázy
- buňky se mohou diferencovat (př. u neuroblastomu) nebo dřímat v „klidovém“ stavu, aniž ztratí proliferační potenciál, nebo mohou dál metastazovat (tzv. metastázy metastáz)
- proliferace metastázy je vázána na přítomnost různých proliferačních (růstových) faktorů, jejichž koncentrace je v různých orgánech rozdílná, stejně jako koncentrace inhibitorů těchto faktorů
- příklady faktorů: PDGF, faktory produkované vlastními nádorovými buňkami, produkty onkogenů – př. TGF-α, EGF, PDGF (c-sis, c-myc, c-erb) mající aktivitu růstových faktorů
- předpokladem růstu metastázy: plynulý přísun živin a O2
- prostá difuze stačí uživit maximálně mikrometastázu o velikosti 1-2 mm!
- větší metastáza – potřebuje vlastní cévní zásobení – to zajistí novotvorba cév: angiogeneze (hypoxie nádoru stimuluje angiogenezi)
Angiogeneze[upravit | editovat zdroj]
- novotvorba cév
- uplatnění za fyziologických okolností (vývoj embrya, hojení ran, menstruační cyklus)
- vícestupňový proces (kaskáda) regulovaný souborem humorálních působků (cytokinů, integrinů, adhezních molekul, proteolytických enzymů aj.)
- za normálních okolností jsou faktory stimulující v rovnováze s faktory angiogenezu inhibujícími, ztráta rovnováhy → porucha
- průběh angiogeneze: nejprve vazodilatace, protažení endotelových buněk, narušení bazální membrány (enzymaticky a mechanicky), únik fibrinogenu a plazminogenu → přeměna na fibrin a plazmin
- endotelové buňky nejprve vytvářejí „pupeny“ na cévě, zvýšená proliferační aktivita endotelií umožňuje růst „výhonku“ na matrici fibrinových vláken
- novotvořená céva se později stabilizuje, aktivují se pericyty, vytváří se bazální membrána a lumen
- migraci endotelií směrem k nádorovému ložisku indukují humorální podněty z nádorových angiogenních bb., produkují kromě faktorů i proteolytické enzymy
- důležitý význam má stromální a endoteliální produkce kolagenázy IV. – rozrušení membrány umožní migraci endotelií (nádorových buňek a metastazování)
- porušenou cévou uniká fibrinogen a plazminogen → vznikají pak extravaskulární depozita fibrinu, ta tvoří dále matrici pro růst novotvořené cévy (popř. nádoru)
- vaskularizace nádorového ložiska umožní perfuzi nádoru a jeho další růst
- jakmile cévy dosáhnou k nádorovému ložisku, uplatní se též parakrinní mechanismy, jimiž se obě populace (nádorové a endoteliální) ovlivňují
- endotelie produkují velký počet mitogenů a motogenů (působků ovlivňujících motilitu) – hl. PDGF, IGF-, IL-6, IL-8 a další
- čili: existuje úzký vztah mezi angiogenezí a tvorbou metastáz
- čím je angiogeneze intenzivnější, tím vyšší je riziko metastáz a horší prognóza nádorového onemocnění
- stupeň angiogeneze může sloužit jako užitečný prognostický faktor
- inhibice angiogeneze – mohla by být jednou z léčebných modalit
Přehled nejdůležitějších angiogenních faktorů[upravit | editovat zdroj]
- FGF (fibroblast growth factor) – růstový faktor pro fibroblasty, výrazný mitogen endotelových buněk, uvolňuje se z aktivovaných T-lymfocytů, makrofágů, nádorových buněk
- VEGF (vascular endothelial growth factor) – růstový faktor pro endotelie, jeho výdej indukuje ve fibroblastech TGF-β, též stimulace produkce MMP
- TNF-α (tumor necrosis factor) – uvolňován z aktivovaných monocytů a makrofágů, uplatní se při degradaci bazální membrány jako aktivátor MMP, podněcuje výdej některých cytokinů (IL-1) a adhezních molekul, indukuje intravaskulární koagulaci a může způsobit uzávěr cévy a nekrózu nádoru
- MMP – metaloproteázy, enzymy, proteolytickým účinkem působí na bazální membránu endotelií a extracelulární matrix, usnadňují angiogenezi vytvářením prostoru pro nově vznikající cévu, podporují invazi bb nádoru do cév (význam pro angiogenezi i metastazování)
- PDGF – mitogen, stimuluje proliferaci fibroblastů a produkci kolagenu, význam pro formování nového lumen cévy
- TGF-α – aktivuje proteinkinázy, stimuluje proliferaci endotelií
- další faktory: angiogenin, angiopoetin, PD-ECGF, IL-1 (stimulace mitogeneze), IL-6 (vliv na migraci nádorových buněk) a další
Anti-angiogenní faktory[upravit | editovat zdroj]
- jejich potlačení umožní angiogenezi
- trombospondin (produkován fibroblasty pod kontrolou supresorového genu p53, při mutaci tohoto genu u rostoucího nádoru se jeho koncentrace snižuje)
- další: angiostatin, endostatin, interferony (α,β) a další
Nádorová imunologie[upravit | editovat zdroj]
- nádorové buňky – mají změněné antigenní složení
- pro kliniku důležité, zda je antigen specifickým markerem pro daný nádor (detekce a monitorování nádoru) a zda může plnit funkci „rejekčního“ antigenu (terapeutické účely)
- imunologické mechanizmy – důležitá součást pochodů, jimiž se organismus brání vzniku zhoubného nádoru, zajišťováno celým komplexem specifických i nespecifických reakcí
- u imunity zprostředkované buňkami má zásadní význam přímý cytotoxický účinek na nádorovou buňku → ten realizován různými imunokompetentními buňkami a jejich produkty, jejichž aktivita je závislá na vzájemných interakcích zprostředkovaných interleukiny a cytokiny
- specifická odpověď – T-lymfocyty, mají heterogenní populaci
- makrofágy: fagocytují a prezentují antigen, po stimulaci začnou vytvářet IL-1 → ten aktivuje Th–lymfocyty (helper) v jejich postupné diferenciaci v buňky produkující IL-2 a další cytokiny
- IL-2 zodpovědný za klonální expanzi subpopulací lymfocytů, včetně Tc-lymfocytů (cytotoxických) – to jsou terminální efektorové buňky, odpovědné za specifickou destrukci nádorové buňky
- dendritické buňky – vznikají z myeloidních prekurzorů účinkem hemopoetických faktorů, hlavní role: buňky prezentující antigen (APC), produkují cytokiny důležité pro primární imunitní reakci (IL-1, IL-6, další IL)
- NK-buňky – velké granulární lymfocyty, patřící do řady T, ale nezávislé na thymu, zabíjí nádorové buňky nebo buňky napadené virem spontánně bez předchozí senzibilizace
- neutrofilní leukocyty – po jejich vstupu do nádorového ložiska (podporovaného selektiny a integriny) uvolňují chemokiny a cytokiny – ty dále modulují reakce mezi humorální a celulární imunitou
- humorální imunitní reakce – význam B-lymfocyty, po stimulaci antigenem a za koordinované účasti pomocných T-lymfocytů vyzrávají v plazmatickou buňku produkující specifické protilátky
- protilátky: buď samy o sobě protinádorový účinek, ale častěji vazbou a aktivací komplementu indukují jeho cytotoxické působení