Principy obrany proti virovým infekcím
Úvod[upravit | editovat zdroj]
Virové infekce jsou onemocnění zapříčiněné působením virů. Viry mohou napadat jak živočichy, tak rostliny i bakterie. Mezi nejznámější virová onemocnění patří Covid-19, chřipka, AIDS, spalničky, neštovice, klíšťová encefalitida a další. Lidský organismus se proti virovým chorobám brání jednak nespecifickými, jednak specifickými obrannými mechanismy. Mechanismy nespecifické imunity slouží k obraně organismu proti potenciálně škodlivým agens bez ohledu na jejich přesnější identifikaci. Mechanismy specifické imunity představují vysoce selektivní reakci zaměřenou na konkrétní agens po jeho přesné identifikaci, jejich vlastností je posilování a urychlování odpovědi při opakovaném setkání s určitým antigenem.
Nespecifická imunita[upravit | editovat zdroj]
Nespecifická imunita zahrnuje velkou řadu mechanizmů – kožní a slizniční bariéru, sekrety produkované epitelovými buňkami, zánětlivou reakci, interferony, zabijácké lymfocyty a systém komplementu.
Zánět[upravit | editovat zdroj]
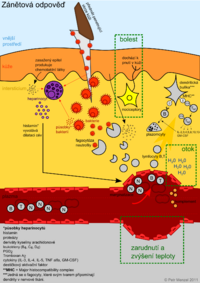
Zánět je komplexní odpověď organismu na poškození tkáně, která nastává po proniknutí infekčních mikroorganismů. Hlavními procesy zánětlivé reakce jsou fagocytóza cizorodých materiálů makrofágy, vazodilatace a zvýšení permeability kapilár a migrace leukocytů do místa zánětu. V místě infekce jsou produkovány cytokiny (mediátory zánětu) a aktivují se kininy. Prvními leukocyty, které putují do tkáně postižené zánětem, jsou neutrofilní granulocyty, s několikahodinovým zpožděním také monocyty, které se rychle transformují na makrofágy. Všechny tyto fagocytující buňky se na místo určení dostávají pečlivě regulovaným postupem, který zahrnuje marginaci, diapedezi a chemotaxi. Marginace je pohyb a přichycení leukocytů k cévní stěně. Diapedeze představuje jejich průnik cévní stěnou, chemotaxe znamená pohyb leukocytů v tkáni směrem k zasaženému místu.
Fagocytóza[upravit | editovat zdroj]
Fagocytóza je schopnost buněk pohlcovat různé částice. Hlavními buňkami, které se účastní fagocytózy, jsou polymorfonukleární leukocyty, monocyty a makrofágy. Fagocytóza se skládá ze čtyř kroků – zachycení cizorodého materiálu, jeho internalizaci, degradaci a exocytózu. Leukocyty rozpoznávají cizorodý materiál díky jeho nepravidelnému povrchu a díky opsoninům, což jsou bílkoviny, které se na tento materiál váží a urychlují jeho identifikaci (opsonizace). Internalizace probíhá procesem endocytózy, poté vlivem trávicích enzymů dochází k degradaci cizorodého materiálu, následně jsou aminokyseliny a další produkty trávení vyloučeny z buňky exocytózou.
Interferony[upravit | editovat zdroj]
Interferony jsou proteiny nespecifické imunity inhibující replikaci virů, které mají parakrinní účinek (tj. na buňky ve svém okolí). Navázáním na membránu okolních buněk zvyšují jejich rezistenci k virové infekci, dále potlačují buněčnou proliferaci, modulují produkci protilátek a buněčnou imunitu, stimulují zvýšenou expresi antigenu histokompatibility, aktivují NK buňky a makrofágy a potencují cytotoxickou aktivitu Tc-lymfocytů.
NK buňky[upravit | editovat zdroj]
NK buňky neboli přirození zabíječi mají nespecifický cytotoxický účinek na morfologicky dosud neporušené buňky. Jejich protivirový efekt spočívá v předčasném přerušení replikačního cyklu.
Komplement[upravit | editovat zdroj]
Komplement je soubor sérových proteinů, jež mají povahu proenzymů a jsou kaskádovitě aktivovány po vazbě C1 na komplex antigen−protilátka, výsledkem je lýza mikroorganismů. Tyto proteiny se v neaktivní podobě vyskytují v krevní plazmě a stykem s některými cukry na povrchu mikrobiální stěny jsou aktivovány.
Specifická imunita[upravit | editovat zdroj]
Prostředky nespecifické imunitní odpovědi jsou velmi účinné, nemusí však vždy zcela eliminovat cizorodý materiál. Proto je důležité, že má organismus k dispozici také mechanismy specifické imunity, které sice nastupují o něco pomaleji, ale mají vysokou účinnost. Na specifické imunitní odpovědi se podílejí jak B-, tak i T-lymfocyty.
B-lymfocyty[upravit | editovat zdroj]
B-lymfocyty se transformují na plazmatické buňky, které secernují specifické protilátky, jež pak kolují v krvi a lymfě, proto se této složce specifické imunitní odpovědi říká humorální imunita.
T-lymfocyty[upravit | editovat zdroj]
T-lymfocyty se transformují na cytotoxické T-buňky, které se přímo vážou na abnormální buňky v těle a následně je likvidují, této složce specifické imunitní odpovědi se proto říká buněčná imunita.
Jak B-, tak i T-lymfocyty reagují na cizorodé molekuly (antigeny). Každý antigen má unikátní strukturu, z níž jsou, z hlediska fungování imunitního systému, nejdůležitější úseky zvané antigenní determinanty (epitopy). Schopnost lymfocytů rozpoznat různé antigenní determinanty je dána přítomností antigenních receptorů na jejich membráně. Tyto receptory vážou specificky vždy jen určitý antigen, jehož antigenní determinanta odpovídá struktuře antigenního receptoru. Při prvním setkání s určitým antigenem nastává primární imunitní odpověď. Při ní dochází k proliferaci a diferenciaci lymfocytů se specifickým antigenním receptorem pro daný antigen vedoucí ke vzniku efektorových buněk (z B-lymfocytů vznikají plazmatické buňky a z T-lymfocytů cytotoxické buňky) – tomuto říkáme tzv. vrozená imunita. Celý proces ovšem trvá přibližně 2 týdny, což sice stačí na likvidaci antigenu, ale obvykle se nezabrání vzniku onemocnění, protože jak bakterie, tak i viry se množí rychleji. Při opakovaném setkání se stejným antigenem paměťové buňky dokážou proliferovat a diferencovat se na efektorové buňky již za 2–7 dní. Díky tomu se při této sekundární imunitní odpovědi nestihnou choroboplodné zárodky rozmnožit a organismus tak vůbec neonemocní – hovoříme o tzv. získané imunitě.
Humorální imunita[upravit | editovat zdroj]
Plazmatické buňky, které vznikly transformací antigenem aktivovaných B-lymfocytů, produkují specifické protilátky. Protilátky jsou bílkovinné molekuly typického tvaru. Skládají se ze čtyř řetězců – dvou těžkých a dvou lehkých. Každá molekula protilátky se skládá z konstantního a variabilního úseku. Konstantní úsek je tvořen těžkými i lehkými řetězci a je zodpovědný za tvar molekuly podobný písmenu Y, ale hlavně je zodpovědný za mechanismus působení protilátky. Existuje celkem 5 různých tříd konstantních úseků a podle toho také máme 5 tříd protilátek (IgM, IgD, IgG, IgE, IgA). Variabilní úsek je na koncových částech obou ramen Y a je rovněž tvořen těžkými i lehkými řetězci. Tento úsek se liší podle antigenu, proti kterému je protilátka namířena, je tedy zodpovědný za její specifický účinek. Protilátky se na likvidaci antigenu podílejí různými způsoby (neutralizací, opsonizaci, aktivací komplementu a aktivací zabijáckých buněk). Neutralizace představuje znemožnění patogenního působení antigenu vazbou protilátky na něj. Nejčastějším mechanismem neutralizace je aglutinace antigenu. Opsonizace usnadňuje fagocytózu, je to proces, při kterém jsou označeny buňky nebo částice určené k fagocytóze.
Buněčná imunita[upravit | editovat zdroj]
Tento typ imunity je zprostředkovávám T-lymfocyty, které na rozdíl od B-lymfocytů potřebují ke své funkci přímý kontakt s infikovanou nebo jinak abnormální buňkou. V těle máme tři hlavní typy lymfocytů. Pomocné T-lymfocyty, které mají regulační funkce a je jich nejvíce. Na svém povrchu nesou CD4, reagují jen v přítomnosti molekul HLA II. třídy. Jejich aktivace vyústí v produkci cytokinů, které pak ovlivňují aktivitu B-lymfocytů, cytotoxických i supresorových T-buněk a zvyšují aktivitu makrofágů i zabijáckých buněk, čímž regulují nespecifickou imunitní odpověď. Cytotoxické (zabijácké) T-lymfocyty na svém povrchu nesou CD8 a reagují pouze v přítomnosti molekul HLA I. třídy. Jsou přímo zodpovědné za buněčnou imunitu, bezprostředně likvidují buňky napadené intracelulárními patogeny (př. viry) a abnormální buňky (př. nádorové buňky). Supresorové T-lymfocyty mají regulační funkce, jsou schopny potlačovat funkce B-lymfocytů, cytotoxických i pomocných T-buněk.
Při virové infekci se vytvářejí protilátky proti rozmanitým virovým antigenům (povrchovým, vnitřním i nestrukturálním) i proti antigenům objevujícím se během množení viru na povrchu infikované buňky. Protilátka proti povrchovým antigenům se váže na virion (základní částice viru schopné infikovat hostitelskou buňku, které jsou složeny z nukleové kyseliny a proteinu), což vede k neutralizaci infekčnosti viru. Navázaná protilátka zabrání přilnutí virionu k receptorům nebo nějak interferuje s jeho průnikem do buňky. Protilátky proti virovým antigenům na povrchu infikované buňky umožňují imunní lýzu nakažených buněk jednak účinkem komplementu, jednak účinkem zabíječských lymfocytů. Zničení infikované buňky dříve, než se z ní uvolní nová generace viru, ochrání další buňky před nákazou.