Krevní skupiny
(přesměrováno z Krevní skupina)
Krevní skupiny se určují podle antigenů na membráně červených krvinek. Jako antigeny se mohou uplatňovat glykolipidy, sacharidy, glykoproteiny nebo proteiny. V současné době se rozlišuje kolem 30 různých systémů krevních skupin.
Nejdůležitější a nejznámější je systém AB0, Rh faktor (negativita matky z hlediska tzv. antigenu D – t.j. Rh faktoru – a pozitivita dítěte může způsobit hemolytickou nemoc novorozenců) a MNS systém, kdy zvláště přítomnost anti-S protilátek u příjemce může způsobit potransfuzní hemolýzu. Dále existuje např. systém antigenu Kell (inkompatibilita může způsobit autoimunitní hemolytickou anémii a hemolytickou nemoc novorozenců). Přítomnost plazmatických protilátek proti antigenům jiným než systémů AB0 a Rh je vzácná, avšak pokud se objeví, může způsobit vážné potransfuzní reakce. Tyto protilátky označujeme jako nepravidelné protilátky.
AB0 (H) systém[upravit | editovat zdroj]
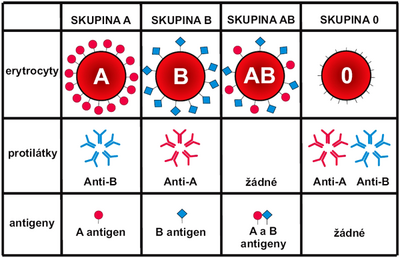
V systému AB0 (H) rozeznáváme čtyři základní typy krevních skupin: A, B, AB a 0. Liší se přítomností aglutinogenů A a B. Ty se nacházejí na povrchu erytrocytu. Jedinec skupiny A má i aglutinogen A a nemá aglutinin Anti-A. Analogicky je tomu i u ostatních krevních skupin. To, že nemá jeden jedinec aglutininy (protilátky) proti vlastním aglutinogenům (antigenům), popisuje Landsteinerovo pravidlo. Jedinec skupiny 0 má aglutininy Anti-A a Anti-B a antigen H, což je antigen vzniklý připojením pouze jednoho monosacharidu na prekurzorovou molekulu. Pokud se na prekurzorovou molekulu nenaváže žádný monosacharid, pak vznikne vzácný antigen Bombay. Antigen A má několik různých forem. Nejvíce zastoupenými v populaci jsou formy A1 (80 %) a A2 (< 20 %).
| Procentuální zastoupení jednotlivých krevních skupin v populaci Evropy[1] | |||
|---|---|---|---|
| 0 | A | B | AB |
| cca 40 % | cca 40 % | cca 10 % | < 10 % |
Rh systém[upravit | editovat zdroj]
Patří mezi nejpolymorfnější a zároveň nejvýznamnější systémy krevních skupin. Byl objeven roku 1939 Karlem Landsteinerem – kazuistika ženy, které byla zjištěna protilátka proti paternálnímu antigenu plodu; tato protilátka byla příčinou potransfuzní reakce na transfuzi krve od jejího manžela a reagovala s přibližně 85 % AB0 kompatibilních krví. O rok později bylo poprvé použito označení Rh na základě izolace protilátky ze séra králíků, kteří byli předtím imunizováni erytrocyty z opice Macacus rhesus. Tento zpočátku jednoduchý systém (označení Rh+/Rh-) se s vývojem vědy rozrostl a v současné době jej tvoří přes 50 antigenů. Z tohoto důvodu je třeba dbát na terminologii a označování krevních skupin – jedinci, na jejichž erytrocytech je přítomen antigen D, se označují jako "RhD pozitivní", v případě nepřítomnosti D antigenu se užívá označení "RhD negativní".
Rh antigeny jsou kódovány dvěma homologními geny: RHCE a RHD. Jejich dědičnost je autozomálně dominantní a jsou umístěné na 1. chromozomu. Přičemž alela D je dominantní k alele d, ale Cc a Ee jsou alelami kodominantními. Ze základních tří párů alel tak lze utvořit 8 možných haplotypů (DCe, dce, DcE, Dce, dcE, dCe, DCE, dCE) a kombinaci 36 odlišných genotypů.
Nejdůležitější z celého systému je antigen D, především kvůli své vysoké imunogenicitě (viz Rh systém).
Rh protilátky: Všechny protilátky tohoto systému jsou považovány za klinicky významné (mají potenciál působit potransfuzní reakce či hemolytickou nemoc novorozence). Většinou jsou to aloprotilátky (vzniklé imunizací), převážně třídy IgG se schopností aktivovat komplement. Optimálně reagují při 37 °C a jejich reaktivitu lze při vyšetření v laboratorním testu zvýšit přidáním enzymu. Nejčastějšími typy aloprotilátek jsou anti-D, anti-C, ev. anti-E a anti-c. Mohou vznikat i autoprotilátky, které se často uplatňují u autoimunní hemolytické anémie (např. auto-anti-e).
[2],
[3]
MNS systém[upravit | editovat zdroj]
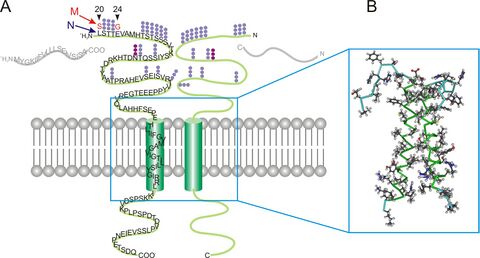
ISBT klasifikace: 002. Patří sem antigeny M, N, S, s a U (+ přes 40 dalších antigenů). Tyto antigeny jsou tvořeny glykoproteiny, obsahujícími kyselinu sialovou, a proto se označují jako sialoglykoproteiny. Antigeny jsou produktem dvou párů alelických genů (GYPA, GYPB). Antigeny MNSs zajišťují elektronegativní potenciál a integritu erytrocytů, jejich interakci s buňkami, jsou receptorem pro cytokiny, bakterie či viry. Zároveň patří do skupiny antigenů, destruovatelných enzymem (např. papain, bromelin, ficin, atd.).
Antigeny M, N[upravit | editovat zdroj]
- jsou dány genem GYPA, který udává vznik glykoforinu A (podle zastoupení a pořadí aminokyselin tak vzniká antigen M a/nebo antigen N
- frekvence fenotypů v kavkazské populaci: M+N+ (50%), M+N- (28%), M-N+ (22%) [3]
- častěji se vyskytují protilátky anti-M (mnohdy jako "přirozené" – susp. poinfekční), anti-N je vzácnější; většinou jsou třídy IgM, reagují za nižších teplot a nejsou klinicky významné (avšak reagují-li v nepřímém antiglobulinovém testu při 37 °C, mohou působit potransfuzní reakci či HON), protilátky reagují silněji s erytrocyty homozygotními pro daný antigen než s heterozygoty
Antigeny S, s[upravit | editovat zdroj]
- jsou dány genem GYPB, udávajícím vznik glykoforinu B (vznik antigenů rovněž závisí na uspořádání aminokyselin)
- řadí se sem i vysokofrekvenční antigen U, který může chybět (v důsledku delece genu) na erytrocytech Afroameričanů s genotypem S-s-U-; jemu korespondující a unikátní protilátkou je anti-U
- frekvence fenotypů v kavkazské populaci: S+s+ (44%), S-s+ (45%), S+s- (11%) [3]
- protilátky bývají typu IgG; optimálně reagují při 37 °C v nepřímém antiglobulinovém testu; jsou považovány za klinicky významné a mohou působit HON či potransfuzní reakce (v případě anti-U až fatální)
Systém P[upravit | editovat zdroj]
ISBT klasifikace: 003;
Správnější je označení P1Pk systém. Od roku 2012 jsou do tohoto systému řazeny tři antigeny: P1, Pk a P1PK4.
Antigeny jsou strukturálně podobné antigenům AB0 systému, kde záleží na působení alelických transferáz a připojování monosacharidů k prekurzorovým řetězcům. V kavkazské populaci má P1 frekvenci 80% (vyšší bývá u Afričanů, nižší naopak v Asii).
P antigen je přítomný i na dalších buňkách, např. na leukocytech, v solubilní formě jej můžeme nalézt v plazmě a v sekretech cyst. Zároveň slouží jako receptor pro bakterie (např. pro parvovirus B19). Účastní se také diferenciace lymfocytů a adheze buněk.
Protilátky jsou většinou třídy IgM, aktivní při nízkých teplotách a bývají klinicky nevýznamné (raritně mírné pozdní potransfuzní reakce, nebyly popsány žádné HON). Významná může být autoprotilátka anti-P, třídy IgG, často nazývaná jako Donath-Landsteinerův hemolyzin. Tato může být příčinou těžké hemolýzy u pacientů s autoimunitní hemolytickou anémií (u paroxyzmální chladové hemoglobinurie).
[2]
Kell systém[upravit | editovat zdroj]
ISBT klasifikace: 006;
Tento systém tvoří více než 30 glykoproteinových antigenů (CD238), které se od sebe liší strukturou proteinu. Je to první systém, objevený pomocí AGH testu (v roce 1946). Svůj název získal podle první popsané kazuistiky – pacientovo příjmení bylo: Kelleher. Antigeny Kell se uplatňují při aktivaci peptidů při vazokonstrikci a mohou být inaktivovány některými chemikáliemi (např. dithiothreitol). Jsou hned po antigenu D nejsilnějšími imunogeny. Nejvýznamnější alelické páry tvoří:
- K (KEL1 neboli Kell; asi 9% populace) a k (KEL2 neboli Cellano; přes 99% populace)
- Kpa (KEL3 neboli Penny) a Kpb (KEL4 neboli Rautenberg)
- Jsa (KEL6 neboli Sutter) a Jsb (KEL7 neboli Matthews)
KEL gen se nachází na 7. chromozomu (7q34) a má spojitost s X-vázaným genem XK, jehož produktem je Kx protein. Pokud tento protein chybí (v důsledku hemizygocie mutace či delece genu XK), jsou všechny antigeny Kell výrazně zeslabené. Imunizované osoby tak mohou vytvářet protilátky anti-Kx a anti-Km. Tento fenotyp je označován jako McLeod (nebo McLeodův syndrom) a bývá pozorován u akantocytózy a svalových či neurologických nemocí.
Vzácně se vyskytuje také nulový fenotyp K0, kde chybí všechny antigeny systému Kell. Osoby s tímto fenotypem mohou po imunizaci vytvářet protilátku anti-K(u), reagující se všemi antigeny Kell systému (kromě fenotypu K0). Byl popsán i fenotyp Kmod, typický pro velmi slabou expresi antigenů Kell systému.
Protilátky jsou klinicky významné s potenciálem výskytu těžkých potransfuzních reakcí a HON (odlišnost od anti-D spočívá v tom, že protilátka anti-Kell působí imunitní destrukci erytroidních progenitorů). Tyto protilátky jsou třídy IgG a vznikají následkem imunizace (ačkoliv byly popsány i případy "přirozených" poinfekčních protilátek). Řadí se mezi tzv. tepelné protilátky a dobře reagují v nepřímém antiglobulinovém testu. Vzhledem k vysoké imunogenitě bývá doporučována transfuzní kompatibilita u dívek a žen ve fertilním věku.
Pozn. Podle doporučení STL JEP musí být všichni dárci krve otypováni na základní Kell antigeny.
[3], [2]
Kidd systém[upravit | editovat zdroj]
ISBT klasifikace: 009;
První protilátka anti-Jka byla detekována roku 1951 v séru Američanky (příjmení Kidd). Nosič těchto antigenů je glykoprotein, jehož funkcí je membránový transport urey. Tyto antigeny jsou součástí i dalších tkání (např. leukocyty, ledviny, mozek, srdce). Tento systém je tvořen alelickým párem kodominantních antigenů Jka a Jkb, určených genem SLC14A1 (18q12.3).
Frekvence v kavkazské populaci: Jk(a+, b+) přes 50%. Vzácně se vyskytuje fenotyp Jk(a-, b-), který je výsledkem homozygocie nefunkčního JK genu. Osoby s tímto fenotypem mohou vytvářet protilátku anti-Jk3.
Antigeny tohoto systému jsou velmi imunogenní a jejich reaktivitu lze zvýšit přidáním enzymu.
Protilátky nebývají časté, ale jsou velmi nebezpečné. Vznikají zpravidla po imunizaci, přičemž však dochází k rychlému zeslabení (rychlá fagocytóza jimi senzibilizovaných erytrocytů). Následkem toho jsou pak obtížně detekovatelné při dalším předtransfuzním vyšetření (někdy reagují jen s homozygotními krvinkami). Řadí se do třídy IgG, ale může se vyskytnout i směs s IgM, která aktivuje komplement. Jsou poté příčinou těžké hemolýzy, jak akutní tak pozdní. Vzácně jsou příčinou HON při fetomaternální inkompatibilitě. Reagují v nepřímém antiglobulinovém testu. Mohou se vyskytovat i autoprotilátky, především v souvislosti s polékovým typem AIHA.
[3], [2]
Duffy systém[upravit | editovat zdroj]
ISBT klasifikace: 008
První protilátka byla detekována roku 1950 v séru polytransfudovaného hemofilika (Mr. Duffy). Glykoprotein Duffy (CD234) nese základní pár alelických antigenů Fya a Fyb. Ty jsou výsledkem exprese genu DARC (1q23.2).
Antigeny systému Duffy slouží jako receptory pro chemokiny a usnadňují invazi některými typy plazmodií (např. původci malárie). V malarických oblastech je tak rozšířen fenotyp Fy (a-b-), který zajišťuje rezistenci erytrocytů k malarické infekci a slouží tak jako přirozený obranný mechanismus. Tento Fynull fenotyp je působen homozygocií pro nulovou alelu – mutace v GATA-1 vázané oblasti promotoru Duffy genu.
Frekvence výskytu: Fy(a+, b+) 49%; Fy(a+, b-) 17%; Fy(a-, b+) 34%.
Slabá forma Fyb je označována jako Fyx. V laboratorních testech při použití enzymů dochází k destrukci antigenů (s výjimkou trypsinu). Známý je také efekt dávky u homozygotních typů.
Protilátky mají charakter IgG, reagují v NAT při 37 °C, bývají směsí aloprotilátek a mohou aktivovat komplement. Bývají málo časté, avšak mají potenciál působit potransfuzní reakce, ojediněle i HON.
[3], [2]
Lewis systém[upravit | editovat zdroj]
ISBT klasifikace: 007
Antigeny tohoto systému byly poprvé popsány v roce 1946. Dva hlavní antigeny tohoto systému Lea a Leb nejsou alelické a jejich vznik je podobný vzniku antigenů u AB0 systému. Produktem genu Le, FUT3 (19p 13.3) je fukosyltransferáza, která mění řetězec H-prekurzoru typu 1 (za vzniku Lea) a/nebo H řetězec typu 1 (za vzniku Leb). Konečný fenotyp tak závisí i na účinnosti genu Se (FUT2).
Syntéza těchto antigenů probíhá v plazmě, sekretech a endodermálních tkáních. Tato Lewis substance (z plazmy) adheruje na erytrocyty a vytváří tak Lewis antigeny (ty tudíž chybí na erytrocytech novorozenců). Síla antigenu se může měnit v těhotenství nebo v souvislosti s onemocněními zažívacího traktu (např. infekce Helicobacter pylori). Antigeny Lewis také fungují jako buněčné ligandy pro E-selektiny.
Nejčastější jsou fenotypy Le(a+, b-) a Le(a-, b+). V přítomnosti genů „le, se“ vzniká fenotyp Le(a-, b-). Varianta Le(a+, b+) je v kavkazské a africké populaci raritní.
Protilátky se řadí mezi tzv. chladové, tudíž reagují při nižších teplotách. Nejsou považovány za klinicky významné, byly však popsány i raritní případy protilátek, reagujících při 37 °C v antiglobulinovém testu a/nebo aktivující komplement, s potenciálem potransfuzní reakce (spíše u anti-Lea).
[3], [2]
| Geny | Fenotyp |
|---|---|
| Le, se, H | Le(a+, b-) |
| Le, Se, H | Le(a-, b+) |
| le, se, H | Le(a-, b-) |
| le, se, hh | Le(a-, b-) |
Lutheran systém[upravit | editovat zdroj]
ISBT klasifikace: 005
Specifita anti-Lua byla popsána roku 1945, anti-Lub o deset let později. V současné době je do tohoto systému řazeno 19 antigenů, přičemž všechny jsou lokalizovány na dvou glykoproteinech (CD239). Tyto proteiny jsou rozdílnými transkripty jednoho genu (gen LU), mají imunoglobulinovou strukturu a patří mezi receptory a adhezivní molekuly (ligandy pro laminin).
Antigeny jsou po narození slabě vyvinuté a zesilují s věkem. Uplatňují se v diferenciaci, adhezi, migraci a proliferaci buněk, při uvolňování zralých erytrocytů do periferní krve. Glykoprotein Lu bývá ve vyšší expresi na maligních buňkách.
Frekvence Lua je v kavkazské a africké populaci okolo 5-8% (jinde je raritní). Oproti tomu Lub se řadí mezi vysokofrekvenční (HFA = High Frequency Antigen) ve všech populacích. Raritně se vyskytuje i nulový fenotyp (Lutheran null), který může být způsoben třemi typy genetických mechanismů:
- homozygocie pro nefunkční LU gen
- heterozygocie pro geneticky nezávislý dominantní regulátorový gen (In/Lu/)
- hemizygozita pro X-vázaný regulátorový gen XS2
Protilátky jsou málo časté jejich klinický význam není příliš velký. Mohou působit mírné pozdní potrasfuzní reakce, ale nejsou spojovány s HON, kvůlu slabé expresi na fetálních krvinkách. Bývají třídy IgM a lépe reagují při nižších teplotách.
[3], [2]
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Reference[upravit | editovat zdroj]
- ↑ http://fyziologie.lf1.cuni.cz/Data/Documents/EB418D61-2403-4EF9-B60E-7B11756B0B23/protokoly_1b_v051.pdf
- ↑ a b c d e f g h PENKA, Miroslav a Eva SLAVÍČKOVÁ, et al. Hematologie a transfuzní lékařství. II, Transfuzní lékařství. 1. vydání. Praha : Grada, 2012. ISBN 978-80-247-3460-6.
- ↑ a b c d e f g h i ŘEHÁČEK, Vít a Jiří MASOPUST, et al. Transfuzní lékařství. 1. vydání. Praha : Grada, 2013. ISBN 978-80-247-4534-3.
- ↑ |popis = struktura glykoforinu A |zdroj = vlastní dílo |datum = 2012-02-27 |autor = Uživatel:Flisk |licence = CC-BY 3.0 CZ
Použitá literatura[upravit | editovat zdroj]
- TROJAN, Stanislav, et al. Lékařská fyziologie. 4., přeprac. a uprav vydání. Praha : Grada, a.s, 2003. 772 s. ISBN 80-247-0512-5.
- ŘEHÁČEK, Vít a Jiří MASOPUST, et al. Transfuzní lékařství. 1. vydání. Praha : Grada, 2013. 237 s. ISBN 978-80-247-4534-3.
- PENKA, Miroslav a Eva SLAVÍČKOVÁ, et al. Hematologie a transfuzní lékařství. II, Transfuzní lékařství. 1. vydání. Praha : Grada, 2012. 192 s. ISBN 978-80-247-3460-6.