Vitamin D
(přesměrováno z Ergokalciferol)
Vitamin D je skupina látek (kalciferolů), které patří mezi vitaminy rozpustné v tucích a hrají nezastupitelnou úlohu v kalciofosfátovém metabolismu, protože jsou nezbytná pro správnou mineralizaci kostí. Jako substance byl poprvé identifikován v kvasinkách a zařazen mezi vitaminy.[1] Vzhledem k tomu, že v organismu dochází k jeho přestavbě (dvojité hydroxylaci) na aktivní metabolit, lze ho nazvat hormonem. Vitamin D je tedy podle novějších poznatků pleiomorfní steroidní hormon, který hraje zásadní roli v rozvoji a údržbě kostní tkáně, svalů, imunity, regulaci a ochraně před srdečními a onkologickými onemocněními.[2]
Ergokalciferol (D2) je rostlinného a cholekalciferol (D3) živočišného původu. Hlavním zdrojem vitaminu D3 je endogenní produkce v kůži, kde vzniká působením ultrafialového záření UVB z provitaminu 7-dehydrocholesterolu. V menší míře je zdrojem vitaminu D rostlinná a živočišná strava či vitaminem D suplementované potraviny. Vzhledem k nedostatečnému příjmu vitaminu D přirozenou potravou mnohé země (mimo ČR) fortifikují vybrané potraviny (mléko, máslo, margaríny, jogurty, některé cereálie) přídavkem vitaminu D2 nebo D3.[1]
Vitamin D2 či D3 (endogenní či ze stravy) je v těle dvakrát hydroxylován, nejprve v játrech a poté v ledvinách, za vzniku kalcitriolu - aktivního metabolitu vitaminu D. Ten je v krvi transportován vázaný na vitamin D vázající protein (DBP) tvořený v játrech. Kalcitriol pak působí přes nitrobuněčný vitamin D receptor (VDR). Má krátký metabolický poločas (cca 4 hodiny).
- Význam vitaminu D
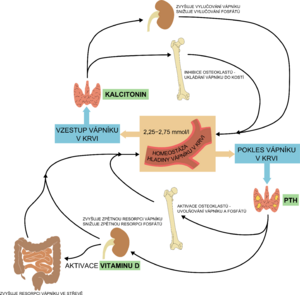
- udržování homeostázy vápníku a fosforu přímým účinkem na střevo, ledviny a kost:
- zvyšuje absorbci kalcia v tenkém střevě a ledvinných tubulech aktivním působením na kalciové kanály;
- reguluje diferenciaci osteoblastů;
- stimuluje expresi alkalické fosfatázy v kostní matrix;
- stimuluje tvorbu osteoklastů (osteoklastogenezi) cestou buněčné interakce s osteoblasty a buněčnými prekursory osteoklastů;
- podporuje mineralizaci kostí;
- inhibuje parathormon, který indukuje kostní resorpci;[2]
- má také řadu extraskeletálních účinků – receptory pro vitamin D (VDR) jsou přítomny ve většině tkání lidského organismu a současně celá řada (extra-renálních) buněk a tkání je schopna hydroxylovat 25-OHD na kalcitriol, nicméně mnohé extraskeletální účinky vitaminu D zatím nebyly podrobněji objasněny;
- přítomnost VDR v makrofázích, dendritických buňkách, T a B lymfocytech podporuje předpoklad významu vitaminu D pro imunitní systém;[3] experimentální studie prokázaly, že úplný deficit vitaminu D vede k těžkým imunopatologiím;[4] snížená hladina vitaminu D je asociována s vyšším výskytem virových infektů horních cest dýchacích;[5][6][7]
- kalcitriol působí na receptory svalových buněk a při nízkých koncentracích (pod 30 nmol/l) klesá významně svalová síla a zvyšuje se riziko pádů u starších žen i mužů;[8]
Denní potřeba se zde pohybuje mezi 200 – 2000 IU, tato hodnota by se neměla dle doporučení překračovat. Výrazně zvýšená potřeba vitaminu D je v průběhu těhotenství. Předávkování vitaminem D je velmi vzácné a prakticky způsobeno vždy arteficiálním podáním léků, pohybujícím se v hodnotách denního příjmu 5000 – 10 000 IU. V nevhodné kombinaci se stravou to může být již hodnota kolem 4 000 IU, kdy v klinickém a laboratorním obraze převažuje výrazně zvýšené kalcium v krvi i v moči.[2] Nadměrná suplementace vitaminu D může vést k rozvoji hyperkalcémie, nefrokalcinózy a tvorbě ledvinných kamenů.[3]
Deficit vitaminu D se pak projeví poruchou mineralizace, tzn. rachitidou u rostoucího organismu, respektive osteomalacií u dospělých. Menší stupeň deficitu vitaminu D vede ke sníženému vstřebávání vápníku s následným poklesem koncentrace vápníku v cirkulaci (především ionizovaného) a s následným vzestupem koncentrace parathormonu (sekundární hyperparathyreóza). Zvýšená koncentrace parathormonu v cirkulaci vystupňuje aktivitu 1-α hydroxylázy s následným vzestupem aktivní formy vitaminu D a současně stimuluje kostní resorpci. Během dětství a dospívání má negativní důsledky i subklinický nedostatek vitaminu D, protože zabrání plnému vývoji kostry (tedy dosahu peak bone mass) a následkem je pak častější výskyt fraktur a osteoporózy.[1]
Mateřské mléko má nízký obsah vitaminu D, proto se u novorozenců doporučuje suplementace vitaminem D3, který se nejen lépe vstřebává, ale má i lepší farmakokinetické a farmakodynamické vlastnosti než vitamin D2. Zdá se, že vitamin D by mohl mít vliv i na imunitní funkce novorozence.[1][9]
Zdroj a metabolismus[upravit | editovat zdroj]
Hlavním zdrojem vitaminu D3 je endogenní produkce v kůži, kde vzniká působením ultrafialového záření UVB (o vlnové délce 290–315 nm) ze 7-dehydrocholesterolu (provitaminu). Množství vitaminu D3 syntetizovaného v kůži závisí na dostupnosti 7-dehydrocholesterolu a na expozici UV záření (roční období, zeměpisná šířka, znečištění vzduchu, používání opalovacích krémů, zahalování těla). Se 7-dehydrocholesterolem soupeří v kůži o fotony UV záření melanin, který tudíž produkci vitaminu D3 snižuje. Lidé s tmavou pletí proto potřebují k vytvoření adekvátního množství vitaminu D delší expozici slunečnímu svitu. V oblastech, ležících nad 40. stupněm severní a pod 40. stupněm jižní zeměpisné šířky v zimních měsících pohybuje slunce nad obzorem v tak nevýhodném úhlu, že vitamin D v kůži prakticky nevzniká. Při dlouhodobé sluneční expozici nedochází k intoxikaci vitaminem D díky fotolytické konverzi provitaminu D3 na tachysterol a lumisterol, což jsou inaktivní metabolity.[4][10]
Vitamin D může být získáván v menší míře také ze stravy. Vitamin D3 je obsažen v oleji z rybích jater, v tučných rybách či ve vaječném žloutku. Vitamin D2 může být syntetizován rostlinami a houbami působením UVB na ergosterol (provitamin). Vitamin D se ze stravy vstřebává v tenkém střevě (v duodenu a jejunu) formou chylomikronů, které se lymfatickým systémem dostávají přes vena cava superior do krevního oběhu.[3]
D2 i D3 jsou biologicky neaktivní a aktivizují se ve dvou krocích (dvoustupňovou hydroxylací): v játrech se mění (enzymem 25-hydroxylázou) na biologicky neaktivní 25-hydroxycholekalciferol (25-OHD, kalcidiol, kalcifediol), který se dále mění převážně v ledvinách ale v menší míře i v jiných tkáních (enzymem 1α-hydroxylázou) na aktivní formu vitaminu D 1,25-dihydroxycholekalciferol (1,25(OH)2D, kalcitriol). Hlavními regulačními faktory hydroxylace jsou hladina parathormonu, fosforu a kalcia. Tato aktivní přestavba, která z vitaminu učiní de facto hormon, probíhá především v ledvinách, potřebnou enzymovou výbavu mají ale mnohé další tkáně, které si mohou „lokálně vyrobit“ aktivní vitamin D pro potřebu vlastních metabolických procesů.[1] K lokální produkci kalcitriolu dochází například uvnitř makrofágů, lymfocytů, placenty, keratinocytů, vlasových folikulů, pankreatu, endotelu, nadledvin, tlustého střeva, prostaty, mozku, mléčná žlázy.[10] Kalcidiol a kalcitriol cirkulují krví především vázané na vitamin D binding protein (DBP). Kalcitriol spouští metabolické děje skrze intracelulární vitamin D receptor (VDR).
| Vitamin D | Parathormon | Kalcitonin | |
|---|---|---|---|
| ledviny | ↑ reabsorpci Ca2+ a fosfátů | ↑ resorpci Ca2+ a exkreci fosfátů, stimuluje produkci kalcitriolu |
↑ vylučování Ca2+, ↑ vylučování fosfátů |
| kost | mineralizace kostí; vysoké hladiny naopak odvápňují |
resorpce kostí (aktivace osteoklastů), kalcemie a fosfatemie stoupá |
inhibice osteoklastů, ukládání Ca2+ do kostí |
| střevo | stimuluje resorpci Ca2+ a fosfátů | stimuluje produkci kalcitriolu → stimuluje resorpci Ca2+ a fosfátů |
– |
Konverze jednotek vitaminu D3 ve zdrojích: 1 µg = 40 IU.
Denní doporučená dávka: Podle DACH 2000[13] je od 1 do 65 let 5 µg, nad 65 let 10 µg. Nová revize amerických doporučených dávek (IOM 2011) předpokládá minimální expozici slunečnímu záření (doporučená prevence kožních malignit ochranou proti slunečnímu záření) doporučuje od 1 do 70 let 15 µg, nad 70 let 20 µg[14].
Denní ztráta kalcia z organismu je asi 200 mg (především močí a kožním povrchem) a ta musí být při vyrovnaném metabolismu denně doplněna. Pokud by byl transport ve střevní stěně zcela pasivní, musel by být denní příjem kalcia alespoň 2,500 mg, aby se z něj (pasivně) vstřebalo potřebných 200 mg. Při aktivním transportu, zajištěném především dostatkem vitaminu D, je vstřebáno cca 16 % z přijaté dávky, což znamená, že pro nahrazení 200 mg ztráty musí být denní příjem kalcia potravou alespoň 1000–1 200 mg.[1]
Stanovení[upravit | editovat zdroj]
Nasycení organismu vitaminem D se hodnotí pomocí sérové koncentrace 25-OHD, který má relativně dlouhý poločas rozpadu (2 až 3 týdny).[4]
Stanovování aktivní formy vitaminu D (1,25(OH)2D) se provádí jen u nefropatií, jinak se nedoporučuje pro jeho krátký poločas rozpadu (4 až 7 hodin) a proto, že jeho sérová koncentrace je významně ovlivněna například parathormonem.[4]
Zlatým standardem je metoda LC-MS/MS (Liquid chromatography-mass spectrometry), ale pro její ekonomickou, přístrojovou a personální náročnost se běžněji používají imunochemické metody.[4]
Konverze jednotek 25-OHD v plasmě: 2,5 nmol/l = 1 ng/ml
Deficit[upravit | editovat zdroj]
Za nedostatek vitaminu D je nejčastěji označována hodnota sérové koncentrace 25-OHD <50 nmol/l, ale u této hodnoty nepanuje jednoznačná shoda. Tato hodnota byla stanovena na základě analýzy vlivu 25-OHD na markery kostního metabolismu, zejm. ve vztahu k parathormonu (PTH). (Klinicky významný deficit vitaminu D vede po nějaké době k elevaci PTH.)[4]
Normální plasmatické hodnoty Ca, P, alkalické fosfatázy (ALP) a parathormonu také svědčí o adekvátním přívodu vitaminu D. Při nedostatku vitaminu D se vstřebává málo vápníku, je vylučován PTH → aktivují se osteoklasty → stoupá ALP v séru. Zvýšené hodnoty parathormonu (sekundární parathyroidismus) se objevují při koncentraci 25OH D 10–25 nmol/l, při nedostatečném přívodu vápníku i do 50 nmol/l[13]
Při nedostatku vitaminu D je porušeno ukládání vápníku do novotvořené kosti a kosti se deformují. Klinickými projevy deficitu vitaminu D jsou rachitis u dětí (deformity dlouhých kostí dolních končetin, kraniotabes, caput quadratum, Harrisonova rýha) a osteomalácie u dospělých (hlavně deformity dlouhých kostí dolních končetin a pánevních kostí). Nedostatek vitaminu D v pozdějším věku také přispívá ke vzniku osteoporózy. Na rozdíl od osteomalacie se u osteoporózy redukuje normálně mineralizovaná kostní hmota, kosti jsou křehké a snadno se lámou, ale nedeformují se. Lze odlišit na rtg.
Klinické projevy deficitu vitaminu D se vyskytují na všech kontinentech, rizikovou skupinou jsou zejména děti do 30 měsíců, nejvíce kojenci – v mateřském mléce je málo vitaminu D, nejsou příliš vystavováni slunečnímu svitu a jejich růst je velmi intenzivní (velká potřeba).
V posledních letech je popisován subklinický nedostatek (nízká hladina 25OHD) u značného procenta obyvatel jak v Severní Americe, tak v Evropě, IOM[14] však poukazuje na neexistenci obecného konsensu o adekvátní hladině plasmatického 25OHD a tak existuje možnost nadhodnocení prevalence deficitu v populaci.
Prevence: V ČR je doporučeno podávání vitaminu D od 2 týdnů v průběhu celého prvního roku a v zimních měsících druhého roku života.
Nadbytek[upravit | editovat zdroj]
Hypervitaminóza se vyskytuje při předávkování potravinovými doplňky. Vede k hyperkalcémii a posléze ke kalcifikaci měkkých tkání – poškození srdce a ledvin.
Nejčastěji dochází k hypervitaminóze u kojenců při nesprávné prevenci rachitis. Symptomy se objeví po 1–3 měsících podávání nadměrného množství vitaminu D: hypotonie, anorexie, iritabilita, polyurie, polydipsie → dehydratace, zácpa, hmatné skybaly v břiše, žízeň, bledost, zvracení.
Horní hranici denního dlouhodobého tolerovatelného příjmu vitaminu D pro dospělé je 50 μg podle DACH 2000[13] a 100 μg podle IOM[14].
Poznámka[upravit | editovat zdroj]
Z evolučního hlediska je vitamin D jedním z nejstarších hormonů, který je produkován i některými z prvních forem života - fytoplanktony.[3]
V posledních letech je věnována značná pozornost možným dalším úlohám vitaminu D v lidském organizmu. Receptory pro vitamín D (VDR) jsou totiž přítomny v těle prakticky všude, i v tkáních, které nemají vztah k homeostáze vápníku a fosforu a genetické studie ukazují, že kalcitriol ovlivňuje transkripci několika stovek genů – 5 % lidského genomu. Na tomto základě někteří odborníci hypotetizují o potenciální preventivní a terapeutické úloze vitaminu D v souvislosti s celou řadou onemocnění (nádorová a autoimunitní onemocnění včetně diabetu 1. typu, diabetu 2. typu, kardiovaskulární onemocněními, hypertenze, infekční onemocnění, neuropsychiatrické poruchy a preeklampsie).
Americký Institute of Medicine (IOM)[14] v roce 2011 po vyčerpávající analýze však konstatoval, že dosavadní důkazy o extraskeletální úloze vitaminu D jsou nekonzistentní a neprůkazné.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
- Vitaminy • Vitaminy rozpustné v tucích • Vitaminy v dietě
- Kalciofosfátový metabolismus • Poruchy kalciofosfátového metabolismu
Reference[upravit | editovat zdroj]
- ↑ a b c d e f PALIČKA, V. Vitamin D: skeletální a extraskeletální účinky. Med. praxi [online]. 2013, roč. 10, vol. 5, s. 199–202, dostupné také z <https://www.medicinapropraxi.cz/pdfs/med/2013/05/07.pdf>.
- ↑ a b c NOVOSAD, P. Vápník a vitamin D u primární a sekundární prevence osteoporózy. Med. praxi [online]. 2017, roč. 14, vol. 5, s. 217–223, dostupné také z <https://www.praktickelekarenstvi.cz/pdfs/lek/2018/89/02.pdf>.
- ↑ a b c d PLUDOWSKI, Pawel, Michael F. HOLICK a William B. GRANT. Vitamin D supplementation guidelines. The Journal of Steroid Biochemistry and Molecular Biology. 2018, roč. ?, vol. 175, s. 125-135, ISSN 0960-0760. DOI: 10.1016/j.jsbmb.2017.01.021.
- ↑ a b c d e f MARATOVÁ, K, et al. Vitamin D a jeho suplementace u dětských pacientů se zánětlivým střevním onemocněním. Pediatrie pro praxi [online]. 2018, roč. 19, vol. 4, s. 190-194, dostupné také z <www.pediatriepropraxi.cz>. ISSN 1213-0494.
- ↑ SABETTA, James R, Paolo DEPETRILLO a Ralph J CIPRIANI, et al. Serum 25-hydroxyvitamin d and the incidence of acute viral respiratory tract infections in healthy adults. PLoS ONE [online]. 2010, vol. 5, no. 6, s. e11088, dostupné také z <https://doi.org/10.1371/journal.pone.0011088>. ISSN 1932-6203.
- ↑ BERGMAN, Peter, Anna-Carin NORLIN a Susanne HANSEN, et al. Vitamin D3 supplementation in patients with frequent respiratory tract infections: a randomised and double-blind intervention study. BMJ Open [online]. 2012, vol. 2, no. 6, s. -, dostupné také z <https://doi.org/10.1136/bmjopen-2012-001663>. ISSN 2044-6055.
- ↑ NORLIN, Anna-Carin, Susanne HANSEN a Emilie WAHREN-BORGSTRÖM, et al. Vitamin D3 Supplementation and Antibiotic Consumption - Results from a Prospective, Observational Study at an Immune-Deficiency Unit in Sweden. PLoS ONE [online]. 2016, vol. 11, no. 9, s. e0163451, dostupné také z <https://doi.org/10.1371/journal.pone.0163451>. ISSN 1932-6203.
- ↑ HRDÝ, P a P NOVOSAD. Nové poznatky o funkci vitaminu D. Prakt. lékáren [online]. 2015, roč. 11, vol. 2, s. 52-54, dostupné také z <https://www.praktickelekarenstvi.cz/pdfs/lek/2015/02/03.pdf>.
- ↑ WALKER, Valencia P, Xiaoran ZHANG a Ida RASTEGAR, et al. Cord blood vitamin D status impacts innate immune responses. J Clin Endocrinol Metab [online]. 2011, vol. 96, no. 6, s. 1835-43, dostupné také z <https://doi.org/10.1210/jc.2010-1559>. ISSN 0021-972X (print), 1945-7197.
- ↑ a b BAYER, M. Vitaminy rozpustné v tucích. Praktické lékárenství [online]. 2008, roč. 4, vol. 5, s. 235-237, dostupné také z <https://www.solen.cz/pdfs/lek/2008/05/10.pdf>.
- ↑ SILBERNAGL, Stefan a Agamemnon DESPOPOULOS. Atlas fyziologie člověka : 6. vydání, zcela přepracované a rozšířené. 3. vydání. Praha : Grada, 2004. s. 290-293. ISBN 80-247-0630-X.
- ↑ LEBL, J, J JANDA a P POHUNEK, et al. Klinická pediatrie. 1. vydání. Galén, 2012. 698 s. s. 189-196. ISBN 978-80-7262-772-1.
- ↑ a b c Deutsche Gesellschaft für Ernährung, Österreichische Gesellschaft für Ernährung, Sweizerische Gesellschaft für Ernährungforschung, Sweizerische Vereinigung für Ernährung. . Referenzwerte für die Nährstoffzufuhr (DACH). 1. vydání. Frankfurt am Main : Umschau/Braus, 2000. 216 s. ISBN 3-8295-7114-3.
- ↑ a b c d ROSS, AC, et al. Dietary Reference Intakes for Calcium and Vitamin D. 1. vydání. Washington D.C : Institute of Medicine (IOM); National Academy of Sciences, 2011. 1132 s. ISBN 978-0-309-16394-1.