Vyšetření moči/chemické
Běžně se v moči kvalitativně zjišťuje bílkovina, glukóza, hemoglobin, ketolátky a žlučová barviva. Tyto součásti se většinou vyskytují i v moči zdravých osob, ale v tak malém množství, že je běžnými zkouškami neprokážeme. Za různých patologických stavů se jejich koncentrace v moči zvyšuje.
Zkumavkové reakce
Dříve se k průkazu patologických součástí moči používaly barevné a srážecí reakce prováděné tzv. „mokrou cestou“ (ve zkumavkách). Souhrnně jsou jejich principy v tabulce:
| Analyt | Princip reakce | Jednotlivé zkoušky |
|---|---|---|
| Bílkovina | denaturace bílkovin |
|
| Hemoglobin | pseudoperoxidázová aktivita hemového železa – katalyzuje oxidaci vhodných chromogenů na barevné produkty
peroxidem vodíku |
|
| Glukóza | nespecifické zkoušky založené na redukčních vlastnostech glukózy |
|
| Ketolátky | reakce s nitroprusidem sodným v alkalickém prostředí za vzniku fialového komplexu | |
| Bilirubin | oxidace bilirubinu na zelený biliverdin nebo modrý bilicyanin |
|
| Urobilinogen | reakce urobilinogenu s 4-dimethylaminobenzaldehydem v kyselém prostředí za vzniku barevného kondenzačního produktu |
Testovací (diagnostické) proužky
Průkaz patologických součástí moči přímo u lůžka nemocného nebo v linii prvního kontaktu s pacientem umožňuje vyšetřování pomocí testovacích proužků.
Testovací proužky jsou tvořeny nosičem z umělé hmoty, na němž jsou upevněny jedna nebo více indikačních zón. Ty jsou vyráběny tak, že do vhodného materiálu (např. speciální filtrační papír) se nasaje kapalné analytické činidlo, které se šetrně vysuší.
Diagnostické proužky se dodávají jako monofunkční, polyfunkční nebo proužky pro speciální vyšetření.
Monofunkční proužky obsahují základní indikační zóny pro semikvantitativní stanovení určité látky v moči. Polyfunkční proužky jsou tvořeny několika indikačními zónami, umožňujícími vyšetření několika biochemických parametrů najednou. Jsou určeny pro případy, kdy je zapotřebí získat co nejvíce informací o zdravotním stavu pacienta, např. při různých screeningových akcích. Kromě monofunkčních a polyfunkčních proužků existují proužky pro speciální vyšetření, kde jsou zařazeny kombinace dvou nebo více indikačních zón, které jsou zvoleny pro vyšetření určitého onemocnění, např. proužky pro screening diabetes mellitus obsahují zónu pro stanovení glukózy, ketolátek, bílkoviny a pH.
Pomocí testovacích proužků lze stanovit tyto parametry v moči:
Principy stanovení jednotlivých parametrů
Bílkovina
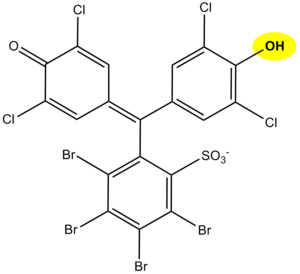
Princip stanovení bílkovin v moči pomocí diagnostických proužků je založen na tzv. bílkovinné chybě acidobazického indikátoru, např. tetrabromfenolové modři, etylesteru tetrabromfenolftaleinu či 3´,3´´,5´,5´´-tetrachlorfenol-3,4,5,6-tetrabromsulfoftaleinu. Jako každý acidobazický indikátor tyto látky při určitém pH mění svou barvu (chovají se jako slabé kyseliny, přičemž protonovaná forma má jiné zbarvení než disociovaná forma): při pH nižším než 3,5 jsou žluté, při vyšším pH jsou zelené až modré. V reakční zóně testovacího proužku je kromě indikátoru i pufr, který udržuje pH v rozmezí 3,0 až 3,5, indikátor tedy má žlutou barvu. Jsou-li ve vzorku bílkoviny, naváží se svými aminoskupinami na indikátor. Tím ovšem změní jeho vlastnosti – přechodová oblast se posune směrem ke kyselejšímu pH. Znamená to, že při uvedeném konstatním pH mezi 3,0 až 3,5 bude mít indikátor s navázanou bílkovinou zelenou barvu, jako kdyby byl v alkaličtějším prostředí (proto bílkovinná chyba indikátoru). Intenzita zbarvení závisí na koncentraci bílkoviny, kolísá od zelené až po modrou a hodnotí se vizuálně nebo instrumentálně.
U výrazně alkalických močí (pH nad 8) nebo je-li moč velmi koncentrovaná, může test dávat falešně pozitivní výsledky (dojde k vyčerpání pufru v reakční zóně). V těchto případech moč okyselíme několika kapkami zředěné kyseliny octové na pH 5–6 a test opakujeme. Falešnou pozitivitu mohou také způsobit vysoké koncentrace některých látek s aminoskupinami (kontaminace odběrové nádoby některými dezinfekčními prostředky), jež se na indikátory váží podobně jako bílkoviny.
Nevýhodou testovacích proužků je jejich rozdílná citlivost vůči jednotlivým bílkovinám. Proužky reagují velmi dobře s albuminem a jeho přítomnost indikují v moči od 0,1 až 0,5 g/l. Podstatně nižší citlivost vykazují vůči globulinům, glykoproteinům a Bence-Jonesově bílkovině. Těmito diagnostickými proužky nelze prokázat zvýšení albuminurie na hodnoty do asi 200 mg/l, resp. denní ztráty albuminu v rozmezí 30 až 300 mg/24 hodin, které provází zejména časnější fáze některých nefropatií. Pro skrínink zvýšení albuminurie je možno použít imunochemických metod, např. speciálních diagnostických proužků založených na imunochromatografickém principu nebo imunoturbidimetrie.
Hemoglobin
Hemoglobin katalyzuje, podobně jako peroxidáza, oxidaci (dehydrogenaci) některých substrátů (např. derivátů benzidinu) peroxidem vodíku:
Nejedná se však o enzymovou aktivitu (katalýzu podmiňuje hemové železo), a proto se neztrácí ani po tepelné denaturaci. Hovoříme o pseudoperoxidázové aktivitě, která se využívá k citlivým, ale nespecifickým důkazům hemoglobinu nebo stopových množství krve. Výhodné je ke sledování reakce použít chromogenní substrát, tj. látku poskytující dehydrogenací výrazně zbarvený produkt (často benzidin nebo jeho nekancerogenní deriváty, aminofenazon apod.).
Reagenční zóna diagnostických proužků obsahuje chromogen (např. tetrametylbenzidin) se stabilizovaným peroxidem vodíku (např. kumenhydroperoxidem). V přítomnosti volného hemoglobinu (hemoglobinurie) se indikační zóna zbarví rovnoměrně modře. Pokud jsou v moči přítomny erytrocyty (erytrocyturie), vytvářejí se intenzivně zelenomodře zbarvené tečky až skvrny.
S hemoglobinurií se můžeme setkat u intravaskulární hemolýzy. K častější erytrocyturii vede jak poškození glomerulární membrány (glomerulární hematurie), tak krvácení z jakékoliv části vývodných cest močových. Často ji nacházíme u infekcí močových cest, urolitiázy a nádorů urogenitálního traktu.
Kromě hemoglobinu poskytuje pseudoperoxidázovou reakci i myoglobin, který se může do moči vylučovat při rozpadu kosterního svalstva (rabdomyolýza, crush-syndrom). Pozitivita zkoušky může být způsobena i peroxidázami leukocytů či některých bakterií, kvasinek nebo plísní, které se mohou vyskytovat v moči zejména při infekcích močových cest. Chceme-li vyloučit možnost falešně pozitivní reakce účinkem buněčných peroxidáz, je nutno reakci provádět s povařenou močí.
Kontaminace odběrové nádoby silnými oxidačními činidly rovněž vyvolává falešnou pozitivitu reakce. Na druhé straně může přítomnost silně redukujících látek (např. kyselina askorbová) zpomalit až zastavit pseudoperoxidázovou reakci a být tak příčinou falešně negativních výsledků.
Glukóza
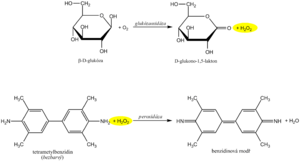
Diagnostické proužky pro průkaz glukózy v moči jsou založeny na principu enzymových reakcí s glukózaoxidázou a peroxidázou (stejný princip jako stanovení glykémie). D-glukóza je pomocí glukózaoxidázy oxidována kyslíkem a vzniká D-glukono-1,5-lakton a peroxid vodíku. V následné peroxidázové reakci peroxid vodíku oxiduje tetrametylbenzidin či jiný chromogen na barevný produkt. Světle žluté zbarvení reakční plošky se při pozitivitě mění na modrozelené. Test je specifický pro D-glukózu, jiné cukry neposkytují pozitivní reakci.
Vysoké koncentrace redukujících látek jako je kyselina askorbová zpomalují vývin zbarvení a mohou vést k falešně nižším výsledkům. V těchto případech se doporučuje opakovat analýzu minimálně 10 hodin po vysazení vitaminu C. Naopak falešně pozitivní výsledky mohou být způsobeny přítomností peroxidu vodíku či oxidačních činidel (některé dezinfekční prostředky) v odběrové nádobě. Stanovení glukózy v moči je nutno provést rychle, aby se zamezilo kontaminaci bakteriemi, nebo moč uchovávat při 4 °C.
Interference s kyselinou askorbovou je častým zdrojem falešných negativit. Diagnostické proužky pro vyšetření moči od některých výrobců jsou proto upraveny tak, aby reakční zóna byla vůči kyselině askorbové alespoň do určité míry odolná. Některé diagnostické proužky také mají detekční zónu pro askorbát, která na možnost falešné negativity upozorní.
Glukosurie nejčastěji provází vzestup glykemie nad tzv. renální práh glukózy (kolem 10 mmol/l). Glukóza, která se normálně filtruje přes glomerulární membránu, je v primitivní moči v tak vysoké koncentraci, že nestačí být resorbována v tubulech a dostává se do definitivní moči. Glukosurie při normální glykemii svědčí pro poruchu tubulárních transportních mechanismů – hovoříme o renální glukózurii.
Ketolátky
Průkaz ketolátek je založen na reakcích kyseliny acetoctové a acetonu s nitroprusidem sodným v alkalickém prostředí, kdy vzniká červenofialově zbarvený komplex[1]. Tento princip využívá Legalova a Lestradetova zkouška, stejně tak jsou na něm postaveny i diagnostické proužky. Kyselina β-hydroxymáselná (tedy nejhojněji zastoupená ketolátka) reakci neposkytuje, a proto negativní výsledek ketoacidózu zcela nevylučuje[2].
Falešnou pozitivitu zkoušek na ketolátky v moči poskytují sloučeniny s volnými sulfhydrylovými skupinami (např. antihypertenzivum kaptopril či uroprotektivum užívané v některých chemoterapeutických schématech mesna)[1]. Poměrně často poskytují podobnou reakci také produkty bakterií při infekcích močových cest.
Falešné negativity kromě již uvedené necitlivosti zkoušek ke kyselině β-hydroxymáselné nejsou významné.
Viz též Ketolátky v moči.
Bilirubin
Průkaz bilirubinu v moči pomocí diagnostických proužků je založen na azokopulační reakci, kterou poskytuje konjugovaný bilirubin se stabilní diazoniovou solí (např. 2,6-dichlorbenzendiazoniumtetrafluoroborát). Vzniká růžové až růžovočervené barvivo. Při současném výskytu vysokých koncentrací urobilinogenu se zbarvení mění do oranžova. V tomto případě se doporučuje vyhodnotit zbarvení až po 2 minutách od namočení indikační zóny. Nižší až falešně negativní výsledky mohou být způsobeny vysokými koncentracemi kyseliny askorbové. Vzorky moči je nutno chránit před přímým slunečním světlem, které vyvolává oxidaci bilirubinu s následným falešně nižším až negativním nálezem.
V moči se vyšetřuje pouze konjugovaný bilirubin, neboť nekonjugovaný bilirubin se do ní nemůže vyloučit.
Urobilinogen
Pro stanovení urobilinogenu v moči se podobně jako u bilirubinu využívá princip azokopulační reakce se stabilní diazoniovou solí (např. 4-metoxybenzendiazoniumtetrafluoroborát). Indikační zóna se barví v přítomnosti urobilinogenu růžově až červeně. Slabě růžové zbarvení odpovídá ještě fyziologickému vylučování urobilinogenu. V přítomnosti bilirubinu je zbarvení žluté, které přechází po 1 minutě do zeleného až modrého odstínu.
Falešnou pozitivitu mohou způsobit některé heterocyklické dusíkaté látky produkované bakteriemi při infekcích močových cest. Falešnou negativitu mohou způsobovat vysoké koncentrace askorbátu.
Leukocyty
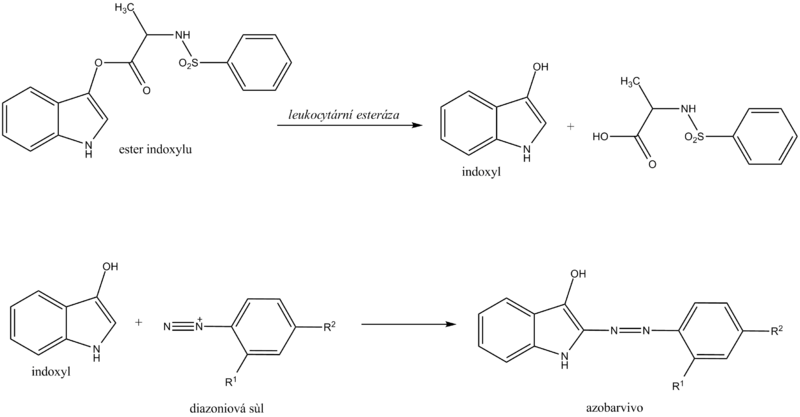
Chemické stanovení leukocytů diagnostickým proužkem je založeno na průkazu esteráz, které jsou hojné v granulocytech. Granulocytární esterázy katalyzují hydrolýzu esteru indoxylu na volný indoxyl. Indoxyl pak reaguje se stabilní diazoniovou solí na příslušné azobarvivo. Při negativní reakci je zóna zbarvena krémově žlutě, při pozitivní reakci se mění do růžového až fialového odstínu.
Vyšetření leukocytů chemickou cestou nenahrazuje mikroskopické vyšetření. Na druhé straně je možné tímto způsobem prokázat i lyzované leukocyty (např. v hypotonické moči), což mikroskopické vyšetření neumožňuje.
Leukocyturie je příznakem zánětu ledvin nebo močových cest. Příčinou většiny pozitivních nálezů bývá bakteriální infekce močových cest. Při pozitivním nálezu leukocytů se doporučuje doplnit vyšetření proteinurie, hematurie, nitriturie, vyšetření močového sedimentu a dále mikrobiologické vyšetření.
Dusitany
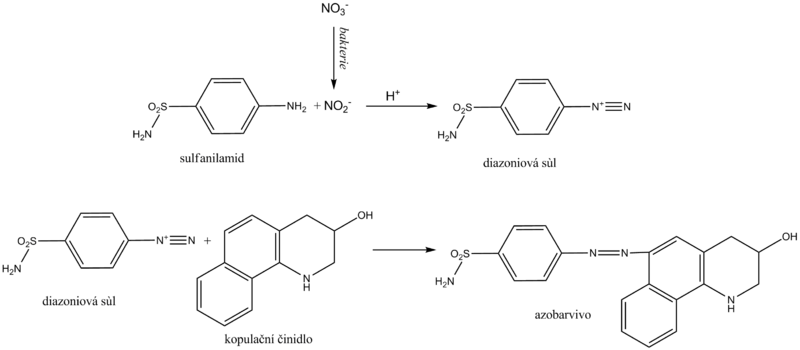
Dusitany se v moči stanovují jako nepřímá známka bakteriurie. Normální moč je v měřitelných koncentracích neobsahuje. Některé především gramnegativní bakterie, jako je Escherichia coli, Proteus, Klebsiella, ale také některé stafylokoky a další, mají schopnost redukovat dusičnany přítomné v moči na dusitany. Diagnostické proužky na nepřímý průkaz bakteriurie využívají dusitanů v tzv. Griessově reakci. Její podstatou je diazotace sulfanilamidu dusitany ve vzorku za vzniku diazoniové soli. Následuje azokopulace vzniklé soli s kopulačním činidlem za vývinu růžového až fialového zbarvení.
Vyšetření moči na dusitany je zapotřebí provádět v první ranní moči, neboť v tomto případě je zaručena dostatečně dlouhá doba nezbytná pro bakteriální redukci dusičnanů na dusitany v močovém měchýři. Dalším doporučením je konzumace dostatku zeleniny (obsahuje dusičnany) den před vyšetřením. Pozitivní průkaz dusitanů v moči potvrzuje bakteriurii, zatímco negativní ji nevylučuje.
Nepřímý průkaz bakteriurie je orientační a nenahrazuje mikrobiologické vyšetření.
Kyselina askorbová
Kyselina askorbová se v moči objevuje při vysokém příjmu potravou. Jako silné redukční činidlo může ovlivnit stanovení některých analytů v moči, zejména těch, které při reakcích využívají peroxid vodíku. Ten je kyselinou askorbovou přímo redukován. Rovněž rychle rozkládá diazoniové sole používané k azokopulačním reakcím.
Princip detekce kyseliny askorbové využívá kyselinu fosfomolybdenovou, která je kyselinou askorbovou redukována na molybdenovou modř. Reakce není specifická pouze pro kyselinu askorbovou, podobně reagují i jiné látky se silnými redukčními účinky.
pH
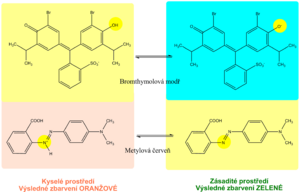
Indikační zóna pro pH obsahuje směs vybraných acidobazických indikátorů. Většina využívá dva acidobazické indikátory – metylovou červeň a bromthymolovou modř, popř. fenolftalein. Tím je zabezpečeno odečítání pH v rozsahu 5–9 změnou barvy z oranžové (kyselé pH) na zelenou až modrou (alkalické pH). Odečet je možný s přesností na 0,5.
Hustota
Relativní hustotou moči rozumíme poměr hustoty moči a hustoty vody. Hustota vody je prakticky rovna 1 kg/l, takže rozdíl mezi hustotou vody (v kg/l) a relativní hustotou moči je zanedbatelný. Hustota má v soustavě SI rozměr kg·m-3. Hustota vzorku vztažená na hustotu vody je relativní veličina a je tedy udána bezrozměrným číslem.
Stanovení hustoty moči
Hustota moči se pomocí diagnostických proužků odhaduje nepřímo podle koncentrace kationtů. Indikační zóna proužku obsahuje vhodný polyelektrolyt ve funkci iontoměniče a acidobazický indikátor bromtymolovou modř. Princip diagnostických proužků je založen na výměně kationtů z moči, zejména Na+, K+, NH4+, za ionty H+ polyelektrolytu v indikační zóně. Uvolněné H+ okyselí slabě pufrovaný acidobazický indikátor, který je v alkalické formě. Okyselení je doprovázeno změnou zbarvení bromtymolové modři. Nevýhodou je, že vyšetření diagnostickými proužky nebere v úvahu látky neelektrolytové povahy jako je glukóza, bílkoviny, močovina, kreatinin a některé další.
Postup při vyšetření diagnostickými proužky
Z tuby vyjmeme jen tolik proužků, kolik budeme bezprostředně potřebovat. Tubu se zbývajícími proužky ihned uzavřeme, abychom nepoužité proužky chránili před vlhkostí. Nedotýkáme se rukou indikační zóny proužků. Proužky uchováváme pouze v originálních obalech a dobře uzavřené se sáčkem se sušidlem, v temnu, na suchém místě při teplotě +2 až +30 °C.
Proužek ponoříme krátce na 1–2 s do vyšetřované moči tak, aby byly všechny zóny smočeny. Poté proužek vyjmeme a přebytek moči odstraníme otřením hrany proužku o okraj nádoby. Pak jej uložíme do vodorovné polohy, aby se zabránilo smíchání činidel z jednotlivých reagenčních plošek. Po uplynutí předepsané reakční doby, obvykle 60 s a pro leukocyty 120 s, vyhodnotíme.
Hodnocení zabarvení reakčních zón diagnostických proužků se provádí:
- subjektivním srovnáním výsledného zbarvení s barevnou stupnicí na štítku tuby, v níž jsou proužky uloženy;
- objektivně pomocí reflexních fotometrů, které měří intenzitu světla vhodné vlnové délky odraženého od reakčního políčka.
Přehled vyšetření moči pomocí diagnostických proužků
| Analyt | Princip | Falešně pozitivní výsledky | Falešně negativní výsledky |
|---|---|---|---|
| Bílkovina | Proteinová chyba acidobazického indikátoru | Alkalické pH, znečištění odběrové nádoby dezinfekčními prostředky na bázi kvarterních amoniových solí, menstruace (nevyšetřujeme 3 dny před a po), hemoglobinurie, myoglobinurie | Globuliny a lehké řetězce imunoglobulinů jsou těžko prokazatelné |
| Hemoglobin | Oxidace chromogenu peroxidem vodíku účinkem pseudoperoxidázové aktivity hemoglobinu | Mikrobiální peroxidázy, kontaminace nádob oxidačními čistícími prostředky | Vysoká koncentrace dusitanů, vitamin C |
| Glukóza | Glukózaoxidázová reakce spřažená s peroxidázovou reakcí | Kontaminace nádob oxidačními čistícími prostředky | Vitamin C, další redukující látky (kyselina gentisová, DOPA), močová infekce |
| Ketolátky | Reakce kyseliny acetoctové a acetonu s nitrprusidem v alkalickém prostředí | Látky s volnými sulfhydrylovými skupinami (např. kaptopril). Některé látky na bázi fenolftaleinu a sulfoftaleinu (laxancia a diagnostika) poskytují v alkalickém prostředí podobné zbarvení. Kyselina fenylpyrohroznová. | β-hydroxybutyrát nereaguje |
| Bilirubin | Azokopulační reakce | Látky, které mají v kyselém prostředí podobné zbarvení, dusíkaté metabolity bakterií u některých močových infekcí | Vysoký obsah dusitanů, expozice světlu, kyselina askorbová |
| Urobilinogen | Azokopulační reakce | Látky, které mají v kyselém prostředí podobné zbarvení, dusíkaté metabolity bakterií u některých močových infekcí | Formaldehyd, expozice světlu, stará moč, kyselina askorbová |
| Dusitany | Griessova reakce – diazotace sulfanilamidu dusitany a následná azokopulace | Bakteriální kontaminace | Nedostatek dusičnanů ve stravě, Gram-pozitivní bakterie, velká diureza, vitamin C |
| Leukocyty | Esterázová aktivita granulocytů a makrofágů | Formaldehyd, alkalické pH, vysoká hustota moči | Vitamin C, některé léky |
| pH | Směs acidobazických indikátorů | Formaldehyd (zdánlivě nižší pH), stará moč (alkalické pH) | |
| Hustota | Iontová výměna kationtů moči za H+, stanovení pH acidobazickým indikátorem | Alkalické pH posouvá výsledky k nižším hodnotám |
Odkazy
Reference
- ↑ a b HOHENBERGER, E.F. a H KIMLING. Compendium urinanalysis. Urinanalysis with test strip [online] . 1. vydání. Mannheim : Roche Diagnostics, 2008. 105 s. Dostupné také z <http://www.diavant.info/diavant/servlet/MDBOutput?fileId=1392>.
- ↑ PLIVA-Lachema Diagnostika. PHAN® diagnostické proužky k vyšetření moče [online]. Poslední revize 2009-12-04, [cit. 2010-03-21]. <https://www.erbalachema.com/cz/>.
Externí odkazy
- DASTYCH, Milan a Jaroslav WINKLER. Automatická analýza moči [online]. Portál Lékařské fakulty Masarykovy univerzity, ©2005. Poslední revize 2011-10-27, [cit. 2011-11-25]. <http://portal.med.muni.cz/clanek-10-automaticka-analyza-moci.html>.
Použitá literatura
- SCHNEIDERKA, Petr, et al. Kapitoly z klinické biochemie. 2. vydání. Praha : Karolinum, 2004. 365 s. ISBN 80-246-0678-X.



![\mathrm{H}_2\mathrm{O}_2 + \mathrm{H}_2\mathrm{A}\ \xrightarrow[\mathrm{nebo\ hemoglobin\ a\ jin\acute{e}\ l\acute{a}tky}]{\mathrm{peroxid\acute{a}zy}}\ 2\ \mathrm{H}_2\mathrm{O} + \mathrm{A}](https://wikimedia.org/api/rest_v1/media/math/render/svg/23377fd4d265df004d50c7657f43bcbbe4cdc8ff)