Přenos elektronů
Úvod[upravit | editovat zdroj]
Jedná se o důležitý děj, který je součástí buněčného dýchání, resp. respiračního řetězce. Dochází při něm k uvolňování energie, která je poté využita ATP–syntázou, schopnou vytvořit více než 100 molekul ATP za 1 sekundu.
V rámci elektron–transportního řetězce jsou využívány vysokoenergetické elektrony, které vznikly v průběhu Krebsova cyklu. Z něho vystupují v podobě NADH a FADH2. Prostřednictvím těchto přenašečů jsou transportovány do řetězce enzymů zanořených do fosfolipidové dvojvrstvy vnitřní membrány mitochondrií. Zde pak dochází k jejich předávání spolu s dalšími redukčními ekvivalenty (vodíkovými protony) mezi jednotlivými enzymovými přenašeči podle vzrůstajícího redox–potenciálu. Předávání redukčních ekvivalentů je podmíněno procesy oxidace a redukce jednotlivých redox–přenašečů, mezi ně patří NAD–dependentní dehydrogenázy, flavoproteiny, cytochromy (viz níže) a molekulární kyslík. Při těchto dějích se získává energie sloužící k přenosu vodíkových protonů H+ z matrix mitochondrií do mezimembránového prostoru. Vzniklá vyšší koncentrace vodíkových iontů (protonového gradientu) následně umožní činnost ATP–syntázy.
V závěru přenosu elektron – transportním řetězcem jsou elektrony předány molekulám plynného kyslíku. V této fázi elektrony již odevzdaly veškerou svou energii při průchodu respiračním řetězcem.
Cytochromy[upravit | editovat zdroj]
Jak již bylo zmíněno, cytochromy jsou látky transportující elektrony vnitřní mitochondriální membránou, čehož dosahují kaskádou vzájemných oxidačně–redukčních reakcí.
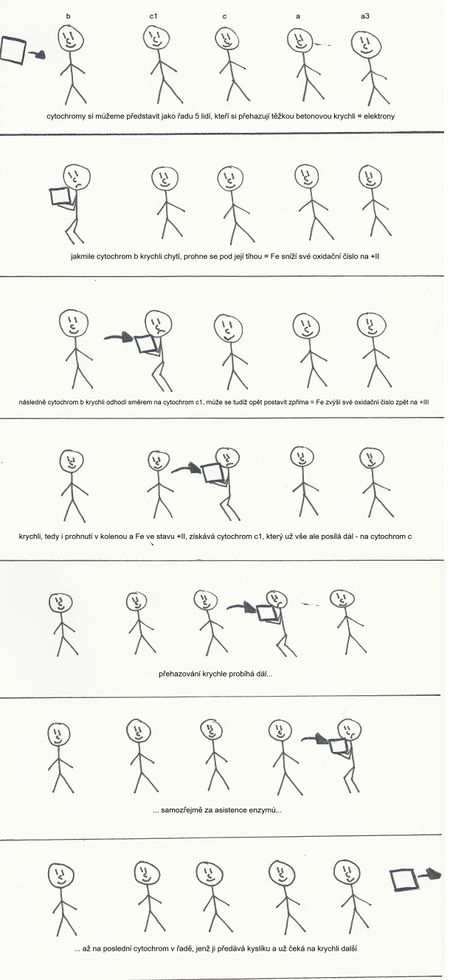
Do dýchacího řetězce jsou zapojeny cytochromy b, c1, c, a, a3 postupně v tomto pořadí podle vzrůstajícího redox–potenciálu, jehož specifickou hodnotu pro daný cytochrom ovlivňuje zejména složení proteinové části molekuly.
Struktura[upravit | editovat zdroj]
Jedná se o hemoproteiny (složené proteiny, jež ke svému řetězci mají navázanou hemovou skupinu), obsahují tudíž železo schopné přecházet mezi dvojmocným a trojmocným stavem, díky čemuž se na přenosu elektronů mohou podílet. Oxidačně–redukční reakcí s předchozím článkem kaskády cytochrom přijme elektron a přítomné železo tak sníží své oxidační číslo na +II, aby ho vzápětí při reakci s článkem následujícím opět odevzdalo a své oxidační číslo tak zvýšilo zpět na +III.
Umístění v buňce[upravit | editovat zdroj]
Cytochromy jsou zabudovány do vnitřní membrány mitochondrií – výjimku tvoří cytochrom c, který je na tuto membránu volně navázán z vnější strany a který je také jako jediný z cytochromů rozpustný ve vodě. Koncovým článkem přenosu elektronů je enzym cytochromoxidáza (obsahující vedle železa i měď), jenž elektrony přenáší na vdechnutý kyslík a podmiňuje tak vznik vody. (detailnější popis reakcí viz Elektronový transportní řetězec)
Vlastnosti[upravit | editovat zdroj]
Cytochromy jsou zkoumány a klasifikovány zejména na základě absorpce záření. Typická absorpční spektra mají zejména v oblasti viditelného světla. (více informací o spektrofotometrii viz Spektrofotometrie)
Nejlépe prozkoumaným je v současné době cytochrom c. Přírodovědci vědí, že se jedná o bílkovinu v sekvenci nesmírně konzervativní, v níž se víc než čtvrtina aminokyselin řetězce nezměnila evolucí ani za 1,5 miliardy let. O ostatních cytochromech mnoho informací známo není.
S cytochromy související onemocnění[upravit | editovat zdroj]
Vzácné genetické onemocnění v angličtině označované jako cytochrome c oxidase deficiency postihuje, jak název napovídá, cytochromoxidázu. V buňkách se jí nenachází dostatek, přenos elektronů a tím i získávání energie pro organismus tudíž není natolik účinné jako u jiných osob. Postiženy jsou zejména tkáně citlivé na nedostatek energie – kosterní svaly, myokard, játra, nervová soustava. Závažnost onemocnění je vysoce variabilní pacient od pacienta.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Použitá literatura[upravit | editovat zdroj]
- ZÁVODSKÁ, Radka. Biologie buněk : základy cytologie, bakteriologie, virologie. 1. vydání. Praha : Scientia, 2006. ISBN 80-86960-15-3.
- MURRAY, Robert K, D. K GRANNER a P. A MAYES, et al. Harperova biochemie. 2. vydání. Praha : H&H, 1998. 872 s. ISBN 80-85787-38-5.
- LEDVINA, Miroslav, Alena STOKLASOVÁ a Jaroslav CERMAN. Biochemie pro studující medicíny. 2. vydání. Praha : Karolinum, 2009. 0 s. ISBN 80-246-0851-0.
- Cytochrome c oxidáze deficiency. In: Genetics Home Reference [online]. November 24, 2014 [cit. 2014-11-29]. Dostupné z: http://ghr.nlm.nih.gov/condition/cytochrome-c-oxidáze-deficiency