Hydrogenuhličitanový pufr
Hydrogenuhličitanový pufrační systém (též bikarbonátový) je nejdůležitějším a nejúčinnějším tlumivým systémem v těle. A to zejména v krvi, kde zastává až 53 % pufrační kapacity.[1] Jeho význam spočívá v dobrých schopnostech udržet stabilní pH především díky tomu, že se koncentrace obou složek může na sobě nezávisle měnit – CO2 dýcháním, HCO3- činností ledvin a jater. Proto se hydrogenuhličitanový pufr v těle označuje jako otevřený pufrační systém.
Reakce probíhá takto: CO2 + H2O HCO3- + H+.
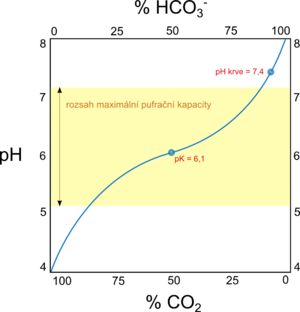
Největší pufrační kapacitu mají pufry složené ze slabých kyselin a jejich solí (resp. slabých zásad a jejich solí) o stejné látkové koncentraci, tedy přesněji, u nichž je pH = pKA. Optimální hodnota pH krve je 7,4 ± 0,04. Hodnota pKA u bikarbonátového pufru je 6,1. Zdá se tedy, že tento pufr nebude moc dobře tlumit výkyvy pH. Opak je ale pravdou. Pro lepší představu se nabízí si uvést příklad:
Do Hendersonovy-Hasselbalchovy rovnice
dosadíme fyziologické koncentrace
- HCO3- = 24 mmol/l a CO2 1,2 mmol/l.
- (Poměr zásady ke kyselině je tedy 20:1.)
Výsledné pH = 7,4.
V případě uzavřeného systému po přidání H+ vzniká konjugovaná kyselina CO2, která nemůže ze systému unikat, a tím pádem její koncentrace stoupá. Vzestup koncentrace CO2 o 2 mmol/l je recipročně vyrovnán poklesem koncentrace HCO3-.
- Výsledné pH = 6,93. (V tomto případě je pufrační kapacita pufru velmi malá, protože hodnota 6,93 je od 7,4 dosti vzdálena.)
Jestliže je však vznikající CO2 ze systému odstraněn (vydýchán), jak je tomu právě v případě hydrogenuhličitanového otevřeného systému, mění se přidáním H+ jen koncentrace HCO3-. Poměr HCO3- a CO2, a tím také hodnota pH, se posune mnohem méně.
- Výsledné pH = 7,36.
Shrnutí: Nárůst H+ v krvi vede k produkci CO2, který je záhy vydýchán v plicích, což umožňuje udržovat konstantní pCO2, tedy koncentraci 1,2 mmol/l.
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Reference[upravit | editovat zdroj]
- ↑ FONTÁNA, Josef. Acidobazická rovnováha [přednáška k předmětu Biochemie, obor Všeobecné lékařství, 3.LF Univerzita Karlova]. Praha. 30.3.2011.
Použitá literatura[upravit | editovat zdroj]
- LEDVINA, M, et al. Biochemie pro studující medicíny II. 2. vydání. Praha : Nakladatelství Karolinum, 2009. 281 s. ISBN 978-80-246-1415-1.



![{\displaystyle pH=pK_{A}+\log {\frac {[HCO_{3}^{-}]}{[CO_{2}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/80928df498a2075049af80b9666618503495bf74)


