Lipoproteiny: Porovnání verzí
m (→Lipoproteiny) |
m (pořadí) značka: editace z Vizuálního editoru |
||
| (Není zobrazeno 100 mezilehlých verzí od 37 dalších uživatelů.) | |||
| Řádek 1: | Řádek 1: | ||
Typickou vlastností většiny [[Lipidy|lipidů]] a [[Steroidy|steroidních]] látek je jejich špatná rozpustnost ve vodném prostředí. V krevní plazmě se proto vyskytují ve formě hydrofilních lipoproteinových částic – komplexů triacylglycerolů (TG), [[cholesterol]]u (CH) a jeho esterů (CHE) s amfifilními fosfolipidy (FL) a bílkovinami. Druhou možností je vazba na [[albumin]]y, ke které dochází v případě volných neesterifikovaných mastných kyselin (NEMK; FFA). | |||
Typickou vlastností většiny lipidů a steroidních látek je jejich | |||
==Struktura lipoproteinové částice== | |||
[[Soubor:Lipoprotein.png|thumb|270px|Lipoproteinová částice]] | |||
Lipoproteiny jsou částice sférického tvaru tvořené jádrem a obalem. | |||
V ''jádře'' lipoproteinové částice jsou soustředěny hydrofobní triacylglyceroly a estery cholesterolu. | |||
''Obal'' je tvořen z molekul polárnějších fosfolipidů a neesterifikovaného [[cholesterol]]u a jedné nebo více molekul specifických bílkovin označovaných apolipoproteiny, zkráceně apoproteiny. Vazba lipidů na proteiny je nekovalentní, takže může snadno docházet k výměně apoproteinů a lipidů mezi jednotlivými částicemi. Apoproteiny označujeme velkými písmeny a pro další členění jsou vyhrazeny římské a arabské číslovky, např. apo A I, apo A II, apo B 100, apo B 48. | |||
Lipoproteinové částice v krvi se liší obsahem lipidové složky a druhem apoproteinu. | |||
==Dělení lipoproteinů== | |||
K dělení lipoproteinů lze využít buď rozdílného obsahu lipidové složky nebo rozdílné velikosti náboje bílkoviny. | |||
*V prvním případě se lipoproteiny dělí [[ultracentrifugace|ultracentrifugací]] na základě rozdílné hustoty závislé na poměru mezi lipidovou a bílkovinnou složkou. Pomocí ultracentrifugace, která je dostupná spíše na výzkumných pracovištích, rozlišujeme tyto základní typy lipoproteinů: | |||
::*chylomikrony; | |||
::*lipoproteiny o velmi nízké hustotě (very low density lipoprotein – VLDL); | |||
::*lipoproteiny o nízké hustotě (low density lipoprotein – LDL); | |||
::*lipoproteiny o střední hustotě (intermediate density lipoprotein – IDL); | |||
::*lipoproteiny o vysoké hustotě (high density lipoprotein – HDL). | |||
*V praxi se však více využívá k dělení lipoproteinových částic [[elektroforéza|elektroforézy]], která je umožněna rozdílnou velikostí náboje bílkovin lipoproteinů. Podle elektroforetické pohyblivosti dělíme lipoproteiny na tyto třídy: | |||
::*chylomikrony; | |||
::*α-lipoproteiny (odpovídají HDL); | |||
::*pre-β-lipoproteiny (odpovídají VLDL); | |||
::*β-lipoproteiny (odpovídají LDL). | |||
*Jinou možností separace je rozdělovací [[chromatografie]]. Dělení lipidů pomocí tenkovrstevné chromatografie (TLC) je založeno na rozdílné rozpustnosti různých lipidů v polárních a nepolárních rozpouštědlech. Mobilní fáze (v našem případě nepolární) se nechá vzlínat póry stacionární tenké vrstvy (silikagel). Mobilní fáze unáší dělené látky ze vzorku, které se více či méně zpožďují interakcí se stacionární fází, a tím se vzájemně rozdělí. | |||
==Přehled lipoproteinových tříd== | |||
====Chylomikrony==== | |||
'''Chylomikrony''' jsou největší lipoproteinové částice s nejnižší hustotou. Při elektroforéze zůstávají na startu a při ultracentrifugaci flotují („plavou” na povrchu). TG představují téměř 90 % z celkové lipidové složky chylomikronů; zbytek tvoří fosfosfolipidy, cholesterol a jeho estery s vyššími mastnými kyselinami. Na bílkoviny připadá kolem 1–2 %. Chylomikrony jsou produktem enterocytů a slouží k transportu triacylglycerolů potravy ze střeva přes lymfatické cesty do krevního řečiště. Působením [[lipoproteinová lipasa|lipoproteinové lipasy]] v endotelu kapilár se z TG chylomikronů uvolňují mastné kyseliny, které jsou dodávány svalům a tukovým buňkám. Součástí chylomikronů je i exogenní cholesterol, který se touto cestou dostává do organismu. Za normálních okolností nejsou po 12 hodinovém lačnění v séru prokazatelné. Jejich přítomnost v krvi se projeví makroskopicky mléčným zkalením séra, které označujeme jako chylózní. Pokud necháme sérum přes noc v lednici, chylomikrony vystoupí na povrch a vytvoří mléčně zkalenou vrstvu na povrchu séra [[Biochemické vyšetření u hyperlipoproteinémie#Chylomikronový test|chylomikronový test]]. | |||
====VLDL==== | |||
'''VLDL (very low density lipoproteins)''' vznikají především v [[játra|játrech]]. Mají o něco vyšší hustotu než chylomikrony. Na lipidovou složku připadá okolo 90 % a na proteiny 10 %. Jádro VLDL je bohaté na triacylglyceroly, které jsou syntetizované v hladkém endoplazmatickém retikulu hepatocytů. V menší míře je do nově vzniklých VLDL zabudován i cholesterol, další molekuly esterů cholesterolu potom získávají od HDL částic v cirkulaci. Úkolem VLDL je poskytovat mastné kyseliny uvolněné z triacylglycerolů působením lipoproteinové lipasy svalům a tukovým buňkám. Po hydrolýze triacylglycerolů [[lipoproteinová lipasa|lipoproteinovou lipasou]] se VLDL mění na IDL a poté na LDL. Přítomnost VLDL v séru se projeví opalescencí. | |||
== | ====LDL==== | ||
'''LDL (low density lipoproteins)''' vznikají z IDL částic po hydrolýze zbývajících triacylglycerolů [[jaterní lipáza|jaterní lipasou]], ale některé jsou uvolňovány do cirkulace játry. Jediným apoproteinem na povrchu je apoprotein B-100. Lipidová složka v nich tvoří téměř 80 % s převažujícím obsahem esterů cholesterolu. Bílkoviny jsou zastoupeny 20%. Proto stoupá i hustota LDL. Jejich hlavní funkcí je transport cholesterolu k buňkám. Odstranění LDL z plazmy se uskutečňuje pomocí LDL receptorů, které jsou lokalizovány na všech buňkách, nejvíce na povrchu hepatocytů. U zdravých osob jsou v LDL částicích obsaženy asi 2/3 celkového cholesterolu. Tato frakce se činí zodpovědnou za usazování cholesterolu v subendoteliálním prostoru cév a tím za rozvoj [[ateroskleróza|aterosklerotických změn]] (LDL; "zlé"; "špatné" částice). Cholesterol v LDL částicích (LDL-cholesterol) se významně uplatňuje při vzniku aterosklerózy. V důsledku zvýšené hladiny LDL v krvi dochází k jejich zvýšenému průniku cévním endotelem do intimy arteriální stěny, kde je různým způsobem modifikována jejich struktura. Modifikované LDL jsou pohlcovány makrofágy, které se přeměňují na tzv. [[pěnové buňky]]. Tento děj je první fází aterosklerotického procesu. Nejvyšší aterogenitou se vyznačují malé denzní LDL, které jsou menší a hustší s průměrem pod 25,5 nm a snadno pronikají endotelem, mají sníženou afinitu k LDL receptorům a snadno podléhají různým přeměnám. Výskyt malých denzních LDL je spojen se zvýšenou koncentrací triacylglycerolů. Stanovení LDL-cholesterolu je zvlášť doporučováno pro vyhodnocení rizika aterosklerózy při zvýšených hladinách celkového cholesterolu a je základem pro rozhodnutí o způsobu a monitorování léčby. | |||
====HDL==== | |||
'''[[HDL]] (high density lipoproteins)''' zajišťují odsun nadbytečného cholesterolu do jater. Jsou produkovány játry, v menší míře i střevem jako tzv. "nascentní" HDL diskovitého tvaru, tvořené pouze fosfolipidovou dvojvrstvou a apoproteiny. Diskovité HDL částice odnímají cholesterol periferním buňkám a přeměňují se na HDL sférického typu bohatého na cholesterol, který je transportován do jater. HDL jsou jako jediné schopny z membrán buněk v subendotelu vyvazovat volný cholesterol a transportovat ho zpátky do jater. Tímto způsobem jsou HDL částice zapojeny do zpětného (reverzního) transportu cholesterolu z periférie do jater, odkud je jako takový vylučován do střeva (HDL cholesterol není využíván pro syntetické či stavební účely). Z toho vyplývá antiaterogenní působení HDL částic (HDL; "hodné"; "dobré" částice). Zvýšená koncentrace HDL-cholesterolu snižuje riziko aterosklerotických změn artérií a naopak snížená koncentrace pod 1,0 mmol/l představuje zvýšené riziko pro rozvoj aterosklerózy. Zvýšení populačního průměru o 10 % sníží výskyt [[ICHS]] o 30–40 %. | |||
''' | ====Lipoprotein (a)==== | ||
'''[[Lipoprotein (a)]]''' je lipoprotein, jehož koncentrace v krvi je dána geneticky. Podobá se částicím LDL, ale na rozdíl od nich je k apoproteinu B100 disulfidovou vazbou připojen ještě zvláštní apoprotein (a), který je částečně homologní s plazminogenem. Zpomaluje a brání aktivaci [[plasminogen]]u na [[plasmin]] a tím blokuje odbourávání fibrinu. Proto má zvýšené koncentrace Lp(a) proaterogenní účinek a koncentrace nad 0,3 g/l jsou pokládány za nezávislý faktor zvyšující riziko aterosklerózy. | |||
{| class="wikitable" | |||
|+'''Charakteristika jednotlivých lipoproteinových tříd''' | |||
|- | |||
!Třída!!Chylomikrony!!VLDL!!IDL!!LDL!!HDL | |||
|- | |||
| align="center" |'''Hustota (g/ml)'''|| align="center" |< 0,94|| align="center" |0,93–1,006|| align="center" |1,006–1,019|| align="center" |1,019–1,063|| align="center" |1,063–1,210 | |||
|- | |||
| align="center" |'''Velikost částic (nm)'''|| align="center" |> 75|| align="center" |25–70|| align="center" |22–24|| align="center" |19–23|| align="center" |4–10 | |||
|- | |||
| align="center" |'''Elektroforetická pohyblivost'''|| align="center" |žádná (zůstávají na startu)|| align="center" |pre-β|| align="center" |pomalé pre-β|| align="center" |β|| align="center" |α | |||
|- | |||
| align="center" |'''Složení''' | |||
|- | |||
| align="center" |'''Lipidy celkem (%)'''|| align="center" |98–99|| align="center" |90–93|| align="center" |89|| align="center" |79|| align="center" |50–55 | |||
|- | |||
| align="center" |'''Triacylglyceroly (%)'''|| align="center" |90|| align="center" |54|| align="center" |20|| align="center" |4|| align="center" |3–5 | |||
|- | |||
| align="center" |'''Neesterifikovaný cholesterol (%)'''|| align="center" |1|| align="center" |7|| align="center" |9|| align="center" |11|| align="center" |6 | |||
|- | |||
| align="center" |'''Estery cholesterolu (%)'''|| align="center" |2|| align="center" |13|| align="center" |34|| align="center" |41|| align="center" |30 | |||
|- | |||
| align="center" |'''Proteiny celkem (%)'''|| align="center" |1–2|| align="center" |7–10|| align="center" |11|| align="center" |21|| align="center" |45–50 | |||
|- | |||
| align="center" |'''Charakteristické apoproteiny'''|| align="center" |A-I, II, IV,B-48, C II, III, E|| align="center" |B-100, C II, III, E|| align="center" |B-100,C-II, III, E|| align="center" |B-100|| align="center" |A-I, II,C-I, II, III, E | |||
|- | |||
| align="center" |'''Místo syntézy'''|| align="center" |střevo|| align="center" |játra|| align="center" |intravaskulárně jako katabolický produkt VLDL|| align="center" |převážně intravaskulárně jako konečný produkt VLDL|| align="center" |játra, střevo, intravaskulárně | |||
|- | |||
| align="center" |'''Funkce'''|| align="center" |transport exogenních triacylglycerolů|| align="center" |transport endogenních triacylglycerolů|| align="center" |transport endogenních triacylglycerolů a esterů cholesterolu|| align="center" |transport cholesterolu do periferních buněk|| align="center" |transport cholesterolu z periferních buněk zpět do jater (reverzní transport cholesterolu) | |||
|} | |||
<noinclude> | |||
<noinclude> | |||
==Odkazy== | |||
===Související články=== | |||
*[[Lipoproteiny (klinika)]] | |||
*[[Biochemické vyšetření u hyperlipoproteinémie]] | |||
*[[Hypolipidemika]] | |||
*[[Hypolipidemická léčba]] | |||
*[[Β-oxidace]] | |||
*[[Lipidy]] | |||
*[[Lipoproteiny]] | |||
[[ | |||
[[ | |||
[[ | |||
===Použitá literatura=== | |||
[[ | * {{Citace | ||
|typ = kniha | |||
|příjmení1 = Burtis | |||
|jméno1 = C.A.|příjmení2 = Ashwood | |||
|jméno2 = E.R | |||
|titul = Tietz Textbook of Clinical Biochemistry | |||
|vydání = 2 | |||
|místo = Philadelphia | |||
|vydavatel = W.B.Saunders Company | |||
|rok = 1994 | |||
|isbn = 0-7216-4472-4 | |||
}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Češka | |||
|jméno1 = R. | |||
|kolektiv = ano | |||
|titul = Cholesterol a ateroskleróza, léčba dyslipidémií | |||
|vydání = 1 | |||
|místo = Praha | |||
|vydavatel = Triton | |||
|rok = 2005 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 80-7254-738-0 | |||
}} | |||
* {{Citace|typ = kniha|příjmení1 = Masopust|jméno1 = J|příjmení2 = |jméno2 = |titul = Klinická biochemie. Požadování a hodnocení biochemických vyšetření I. a II. část|vydání = 1| místo = Praha|vydavatel = Karolinum|rok = 1998|isbn = 80-7184-650-3 | |||
}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Racek | |||
|jméno1 = J. | |||
|příjmení2 = | |||
|jméno2 = | |||
|příjmení3 = | |||
|jméno3 = | |||
|kolektiv = ano | |||
|titul = Klinická biochemie | |||
|vydání = První | |||
|místo = Praha | |||
|vydavatel = Galén – Karolinum | |||
|rok = 1999 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 80-7262-023-1 | |||
}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Schneiderka | |||
|jméno1 = P. | |||
|příjmení2 = | |||
|jméno2 = | |||
|příjmení3 = | |||
|jméno3 = | |||
|kolektiv = ano | |||
|titul = Kapitoly z klinické biochemie | |||
|vydání = 2 | |||
|místo = Praha | |||
|vydavatel = Karolinum | |||
|rok = 2004 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 80-246-0678-X}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Soška | |||
|jméno1 = V | |||
|příjmení2 = | |||
|jméno2 = | |||
|příjmení3 = | |||
|jméno3 = | |||
|kolektiv = | |||
|titul = Poruchy metabolismu lipidů. Diagnostika a léčba | |||
|vydání = 1 | |||
|místo = Praha | |||
|vydavatel = Grada Publishing | |||
|rok = 2001 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 80-247-0234-7 | |||
}} | |||
* {{Citace|typ = kniha|příjmení1 = Štern|jméno1 = P.|příjmení2 = |jméno2 = |kolektiv = ano | |||
|titul = Obecná a klinická biochemie pro bakalářské obory studia.|vydání = 1|místo = Praha|vydavatel = Karolinum|rok = 2005|isbn = 978-80-246-1025-2 | |||
}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Táborská | |||
|jméno1 = E. | |||
|příjmení2 = | |||
|jméno2 = | |||
|příjmení3 = | |||
|jméno3 = | |||
|kolektiv = ano | |||
|titul = Biochemie II – Praktická cvičení | |||
|vydání = 3 | |||
|místo = Brno | |||
|vydavatel = Masarykova universita | |||
|rok = 1999 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 978-80-210-4516-3 | |||
}} | |||
* {{Citace | |||
|typ = kniha | |||
|korporace = | |||
|příjmení1 = Zima | |||
|jméno1 = T. | |||
|příjmení2 = | |||
|jméno2 = | |||
|příjmení3 = | |||
|jméno3 = | |||
|kolektiv = ano | |||
|titul = Laboratorní diagnostika | |||
|vydání = 1 | |||
|místo = Praha | |||
|vydavatel = Galén – Karolinum | |||
|rok = 2002 | |||
|strany = | |||
|edice = | |||
|svazek = | |||
|isbn = 80-7262-201-3 | |||
}} | |||
===Externí odkazy=== | |||
*[[wikipedia:cs:Lipoproteiny|Lipoproteiny (česká wikipedie)]] | |||
*[[wikipedia:en:Lipoprotein|Lipoprotein (anglická wikipedie)]] | |||
</noinclude> | |||
[[Kategorie:Biochemie]] | [[Kategorie:Biochemie]] | ||
[[Kategorie:Endokrinologie]] | |||
[[Kategorie:Fyziologie]] | |||
Aktuální verze z 14. 1. 2025, 22:45
Typickou vlastností většiny lipidů a steroidních látek je jejich špatná rozpustnost ve vodném prostředí. V krevní plazmě se proto vyskytují ve formě hydrofilních lipoproteinových částic – komplexů triacylglycerolů (TG), cholesterolu (CH) a jeho esterů (CHE) s amfifilními fosfolipidy (FL) a bílkovinami. Druhou možností je vazba na albuminy, ke které dochází v případě volných neesterifikovaných mastných kyselin (NEMK; FFA).
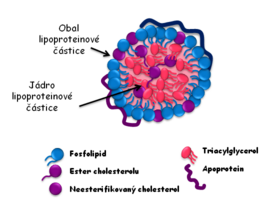
Struktura lipoproteinové částice[upravit | editovat zdroj]
Lipoproteiny jsou částice sférického tvaru tvořené jádrem a obalem.
V jádře lipoproteinové částice jsou soustředěny hydrofobní triacylglyceroly a estery cholesterolu.
Obal je tvořen z molekul polárnějších fosfolipidů a neesterifikovaného cholesterolu a jedné nebo více molekul specifických bílkovin označovaných apolipoproteiny, zkráceně apoproteiny. Vazba lipidů na proteiny je nekovalentní, takže může snadno docházet k výměně apoproteinů a lipidů mezi jednotlivými částicemi. Apoproteiny označujeme velkými písmeny a pro další členění jsou vyhrazeny římské a arabské číslovky, např. apo A I, apo A II, apo B 100, apo B 48.
Lipoproteinové částice v krvi se liší obsahem lipidové složky a druhem apoproteinu.
Dělení lipoproteinů[upravit | editovat zdroj]
K dělení lipoproteinů lze využít buď rozdílného obsahu lipidové složky nebo rozdílné velikosti náboje bílkoviny.
- V prvním případě se lipoproteiny dělí ultracentrifugací na základě rozdílné hustoty závislé na poměru mezi lipidovou a bílkovinnou složkou. Pomocí ultracentrifugace, která je dostupná spíše na výzkumných pracovištích, rozlišujeme tyto základní typy lipoproteinů:
- chylomikrony;
- lipoproteiny o velmi nízké hustotě (very low density lipoprotein – VLDL);
- lipoproteiny o nízké hustotě (low density lipoprotein – LDL);
- lipoproteiny o střední hustotě (intermediate density lipoprotein – IDL);
- lipoproteiny o vysoké hustotě (high density lipoprotein – HDL).
- V praxi se však více využívá k dělení lipoproteinových částic elektroforézy, která je umožněna rozdílnou velikostí náboje bílkovin lipoproteinů. Podle elektroforetické pohyblivosti dělíme lipoproteiny na tyto třídy:
- chylomikrony;
- α-lipoproteiny (odpovídají HDL);
- pre-β-lipoproteiny (odpovídají VLDL);
- β-lipoproteiny (odpovídají LDL).
- Jinou možností separace je rozdělovací chromatografie. Dělení lipidů pomocí tenkovrstevné chromatografie (TLC) je založeno na rozdílné rozpustnosti různých lipidů v polárních a nepolárních rozpouštědlech. Mobilní fáze (v našem případě nepolární) se nechá vzlínat póry stacionární tenké vrstvy (silikagel). Mobilní fáze unáší dělené látky ze vzorku, které se více či méně zpožďují interakcí se stacionární fází, a tím se vzájemně rozdělí.
Přehled lipoproteinových tříd[upravit | editovat zdroj]
Chylomikrony[upravit | editovat zdroj]
Chylomikrony jsou největší lipoproteinové částice s nejnižší hustotou. Při elektroforéze zůstávají na startu a při ultracentrifugaci flotují („plavou” na povrchu). TG představují téměř 90 % z celkové lipidové složky chylomikronů; zbytek tvoří fosfosfolipidy, cholesterol a jeho estery s vyššími mastnými kyselinami. Na bílkoviny připadá kolem 1–2 %. Chylomikrony jsou produktem enterocytů a slouží k transportu triacylglycerolů potravy ze střeva přes lymfatické cesty do krevního řečiště. Působením lipoproteinové lipasy v endotelu kapilár se z TG chylomikronů uvolňují mastné kyseliny, které jsou dodávány svalům a tukovým buňkám. Součástí chylomikronů je i exogenní cholesterol, který se touto cestou dostává do organismu. Za normálních okolností nejsou po 12 hodinovém lačnění v séru prokazatelné. Jejich přítomnost v krvi se projeví makroskopicky mléčným zkalením séra, které označujeme jako chylózní. Pokud necháme sérum přes noc v lednici, chylomikrony vystoupí na povrch a vytvoří mléčně zkalenou vrstvu na povrchu séra chylomikronový test.
VLDL[upravit | editovat zdroj]
VLDL (very low density lipoproteins) vznikají především v játrech. Mají o něco vyšší hustotu než chylomikrony. Na lipidovou složku připadá okolo 90 % a na proteiny 10 %. Jádro VLDL je bohaté na triacylglyceroly, které jsou syntetizované v hladkém endoplazmatickém retikulu hepatocytů. V menší míře je do nově vzniklých VLDL zabudován i cholesterol, další molekuly esterů cholesterolu potom získávají od HDL částic v cirkulaci. Úkolem VLDL je poskytovat mastné kyseliny uvolněné z triacylglycerolů působením lipoproteinové lipasy svalům a tukovým buňkám. Po hydrolýze triacylglycerolů lipoproteinovou lipasou se VLDL mění na IDL a poté na LDL. Přítomnost VLDL v séru se projeví opalescencí.
LDL[upravit | editovat zdroj]
LDL (low density lipoproteins) vznikají z IDL částic po hydrolýze zbývajících triacylglycerolů jaterní lipasou, ale některé jsou uvolňovány do cirkulace játry. Jediným apoproteinem na povrchu je apoprotein B-100. Lipidová složka v nich tvoří téměř 80 % s převažujícím obsahem esterů cholesterolu. Bílkoviny jsou zastoupeny 20%. Proto stoupá i hustota LDL. Jejich hlavní funkcí je transport cholesterolu k buňkám. Odstranění LDL z plazmy se uskutečňuje pomocí LDL receptorů, které jsou lokalizovány na všech buňkách, nejvíce na povrchu hepatocytů. U zdravých osob jsou v LDL částicích obsaženy asi 2/3 celkového cholesterolu. Tato frakce se činí zodpovědnou za usazování cholesterolu v subendoteliálním prostoru cév a tím za rozvoj aterosklerotických změn (LDL; "zlé"; "špatné" částice). Cholesterol v LDL částicích (LDL-cholesterol) se významně uplatňuje při vzniku aterosklerózy. V důsledku zvýšené hladiny LDL v krvi dochází k jejich zvýšenému průniku cévním endotelem do intimy arteriální stěny, kde je různým způsobem modifikována jejich struktura. Modifikované LDL jsou pohlcovány makrofágy, které se přeměňují na tzv. pěnové buňky. Tento děj je první fází aterosklerotického procesu. Nejvyšší aterogenitou se vyznačují malé denzní LDL, které jsou menší a hustší s průměrem pod 25,5 nm a snadno pronikají endotelem, mají sníženou afinitu k LDL receptorům a snadno podléhají různým přeměnám. Výskyt malých denzních LDL je spojen se zvýšenou koncentrací triacylglycerolů. Stanovení LDL-cholesterolu je zvlášť doporučováno pro vyhodnocení rizika aterosklerózy při zvýšených hladinách celkového cholesterolu a je základem pro rozhodnutí o způsobu a monitorování léčby.
HDL[upravit | editovat zdroj]
HDL (high density lipoproteins) zajišťují odsun nadbytečného cholesterolu do jater. Jsou produkovány játry, v menší míře i střevem jako tzv. "nascentní" HDL diskovitého tvaru, tvořené pouze fosfolipidovou dvojvrstvou a apoproteiny. Diskovité HDL částice odnímají cholesterol periferním buňkám a přeměňují se na HDL sférického typu bohatého na cholesterol, který je transportován do jater. HDL jsou jako jediné schopny z membrán buněk v subendotelu vyvazovat volný cholesterol a transportovat ho zpátky do jater. Tímto způsobem jsou HDL částice zapojeny do zpětného (reverzního) transportu cholesterolu z periférie do jater, odkud je jako takový vylučován do střeva (HDL cholesterol není využíván pro syntetické či stavební účely). Z toho vyplývá antiaterogenní působení HDL částic (HDL; "hodné"; "dobré" částice). Zvýšená koncentrace HDL-cholesterolu snižuje riziko aterosklerotických změn artérií a naopak snížená koncentrace pod 1,0 mmol/l představuje zvýšené riziko pro rozvoj aterosklerózy. Zvýšení populačního průměru o 10 % sníží výskyt ICHS o 30–40 %.
Lipoprotein (a)[upravit | editovat zdroj]
Lipoprotein (a) je lipoprotein, jehož koncentrace v krvi je dána geneticky. Podobá se částicím LDL, ale na rozdíl od nich je k apoproteinu B100 disulfidovou vazbou připojen ještě zvláštní apoprotein (a), který je částečně homologní s plazminogenem. Zpomaluje a brání aktivaci plasminogenu na plasmin a tím blokuje odbourávání fibrinu. Proto má zvýšené koncentrace Lp(a) proaterogenní účinek a koncentrace nad 0,3 g/l jsou pokládány za nezávislý faktor zvyšující riziko aterosklerózy.
| Třída | Chylomikrony | VLDL | IDL | LDL | HDL |
|---|---|---|---|---|---|
| Hustota (g/ml) | < 0,94 | 0,93–1,006 | 1,006–1,019 | 1,019–1,063 | 1,063–1,210 |
| Velikost částic (nm) | > 75 | 25–70 | 22–24 | 19–23 | 4–10 |
| Elektroforetická pohyblivost | žádná (zůstávají na startu) | pre-β | pomalé pre-β | β | α |
| Složení | |||||
| Lipidy celkem (%) | 98–99 | 90–93 | 89 | 79 | 50–55 |
| Triacylglyceroly (%) | 90 | 54 | 20 | 4 | 3–5 |
| Neesterifikovaný cholesterol (%) | 1 | 7 | 9 | 11 | 6 |
| Estery cholesterolu (%) | 2 | 13 | 34 | 41 | 30 |
| Proteiny celkem (%) | 1–2 | 7–10 | 11 | 21 | 45–50 |
| Charakteristické apoproteiny | A-I, II, IV,B-48, C II, III, E | B-100, C II, III, E | B-100,C-II, III, E | B-100 | A-I, II,C-I, II, III, E |
| Místo syntézy | střevo | játra | intravaskulárně jako katabolický produkt VLDL | převážně intravaskulárně jako konečný produkt VLDL | játra, střevo, intravaskulárně |
| Funkce | transport exogenních triacylglycerolů | transport endogenních triacylglycerolů | transport endogenních triacylglycerolů a esterů cholesterolu | transport cholesterolu do periferních buněk | transport cholesterolu z periferních buněk zpět do jater (reverzní transport cholesterolu) |
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
- Lipoproteiny (klinika)
- Biochemické vyšetření u hyperlipoproteinémie
- Hypolipidemika
- Hypolipidemická léčba
- Β-oxidace
- Lipidy
- Lipoproteiny
Použitá literatura[upravit | editovat zdroj]
- BURTIS, C.A. a E.R ASHWOOD. Tietz Textbook of Clinical Biochemistry. 2. vydání. Philadelphia : W.B.Saunders Company, 1994. ISBN 0-7216-4472-4.
- ČEŠKA, R., et al. Cholesterol a ateroskleróza, léčba dyslipidémií. 1. vydání. Praha : Triton, 2005. ISBN 80-7254-738-0.
- MASOPUST, J. Klinická biochemie. Požadování a hodnocení biochemických vyšetření I. a II. část. 1. vydání. Praha : Karolinum, 1998. ISBN 80-7184-650-3.
- RACEK, J., et al. Klinická biochemie. První vydání. Praha : Galén – Karolinum, 1999. ISBN 80-7262-023-1.
- SCHNEIDERKA, P., et al. Kapitoly z klinické biochemie. 2. vydání. Praha : Karolinum, 2004. ISBN 80-246-0678-X.
- SOŠKA, V. Poruchy metabolismu lipidů. Diagnostika a léčba. 1. vydání. Praha : Grada Publishing, 2001. ISBN 80-247-0234-7.
- ŠTERN, P., et al. Obecná a klinická biochemie pro bakalářské obory studia.. 1. vydání. Praha : Karolinum, 2005. ISBN 978-80-246-1025-2.
- TÁBORSKÁ, E., et al. Biochemie II – Praktická cvičení. 3. vydání. Brno : Masarykova universita, 1999. ISBN 978-80-210-4516-3.
- ZIMA, T., et al. Laboratorní diagnostika. 1. vydání. Praha : Galén – Karolinum, 2002. ISBN 80-7262-201-3.