Uživatel:Pau/Pískoviště
Hemoglobin a jeho deriváty[upravit | editovat zdroj]
Hemoglobin je červené krevní barvivo, které zajišťuje transport kyslíku z plic do tkání a transport CO2 a protonů z periferních tkání do dýchacích orgánů.
Je to tetramerní protein tvořený čtyřmi podjednotkami. Vždy dvě a dvě podjednotky jsou identické. Ve fyziologicky se vyskytujících hemoglobinech jsou zastoupeny čtyři typy polypeptidových řetězců α, β, γ, a δ, které se liší počtem a sledem aminokyselin. Tetramer je tvořen dvěma α řetězci a dvěma dalšími typy řetězců, které udávají charakter celé molekuly hemoglobinu. U dospělých převládá hemoglobin A, na jehož struktuře se podílejí kromě dvou α řetězců (141 aminokyselin) dva β řetězce (146 aminokyselin).
Součástí každé podjednotky je polypeptidový řetězec, na který je navázán kovalentně jeden hem.
Základem molekuly hemu je protoporfyrin, tvořený 4 pyrrolovými jádry spojenými methenylovými můstky s centrálně vázaným železem. Hemové železo je celkově šestivazné - čtyřmi koordinačními vazbami je spojeno s atomy dusíku pyrrolových jader. Další koordinační valencí se železo váže s imidazolovou skupinou aminokyseliny histidinu v globinovém řetězci. Šestá valence Fe je určena pro molekulu kyslíku (O2).
Hemoglobin v krvi[upravit | editovat zdroj]
Stanovení hemoglobinu v krvi patří k nejzákladnějším laboratorním vyšetřením. Koncentrace hemoglobinu v krvi je hlavním kritériem pro posouzení, zda jde o anemii. Termín anemie (chudokrevnost) se používá při poklesu hemoglobinu nebo erytrocytů pod dolní limit fyziologických hodnot. Anemie patří k velmi častým klinickým nálezům. Jde o stav, který vede ke snížení vazebné kapacity pro kyslík a k následné poruše tkáňového dýchání.
Anemie vzniká za situace, kdy erytropoéza není schopna krýt požadavky na tvorbu nových červených krvinek. Vyvíjí se v důsledku krevních ztrát nebo zvýšeného zániku červených krvinek či nedostatečné tvorby červených krvinek. Následující přehled uvádí některé konkrétní příčiny anémií:
- 1. Anemie ze zvýšených ztrát krve:
- Akutní ztráta krve
- Chronická ztráta krve
- 2.Anemie ze zvýšeného rozpadu erytrocytů (hemolytické stavy)
- Autoimunitní hemolytické anemie (přítomnost protilátek proti vlastním erytrocytům)
- Porucha membrány erytrocytů (odchylka ve složení erytrocytové membrány)
- Dědičné enzymové defekty erytrocytů (pyruvátkinasa, glukosa-6-fosfátdehydrogenasa)
- Nestabilní hemoglobiny - hemoglobinopatie (např. hemoglobin S u srpkovité anemie)
- 3.Anemie ze snížené tvorby erytrocytů
- Nedostatek látek potřebných pro erytropoézu (nedostatek železa, nedostatek vitaminu B12, nedostatek kyseliny listové, nedostatek erytropoetinu - chronická renální onemocnění, nedostatek dalších látek např. vitaminů B1, B6)
- Anemie v důsledku chemického, fyzikálního a radiačního poškození
- Anemie při chronických zánětlivých, infekčních a nádorových onemocněních
Zvýšení hodnot hemoglobinu může být projevem dehydratace organismu nebo chronicky snížené plicní ventilace. Vzácně může být způsobena některými myeloproliferativními stavy, např. polycytemia vera.
Princip stanovení:
- Fotometrické stanovení je založeno na oxidaci dvojmocného železa v hemoglobinu hexakyanoželezitanem draselným na trojmocné železo. Vzniklý methemoglobin se v další reakci s kyanidem draselným přeměňuje na velmi stálý kyanmethemoglobin s jediným širokým absorpčním maximem ve viditelné oblasti při 540 nm.
Hodnocení: Referenční rozmezí koncentrace hemoglobinu v krvi(B hemoglobin)pro dospělého muže je 130 – 180 g/l a pro ženu 120 – 160 g/l. Úkol: Stanovení koncentrace hemoglobinu v krvi - pdf
Hemoglobin v moči[upravit | editovat zdroj]
Močí zcela zdravých lidí se vyloučí až milión erytrocytů za den. Toto velmi malé množství nelze prokázat běžnými chemickými zkouškami. Výskyt většího množství erytrocytů (hematurie) nebo průnik volného hemoglobinu, příp. svalového myoglobinu, do definitivní moči (hemoglobinurie, resp. myoglobinurie) je téměř vždy patologickým nálezem. Moč s nadměrnou příměsí hemoglobinu má narůžovělé až masové zbarvení a spektroskopicky v ní lze prokázat hemoglobin; u masivní hemoglobinurie může nabýt až zbarvení černého piva (degradace hemoglobinu na hematin).
- Hematurie je nálezem, kterému je třeba věnovat patřičnou pozornost, neboť může být příznakem závažného onemocnění uropoetického traktu. Krev v moči může být renálního nebo extrarenálního původu. Je příznakem zánětlivých onemocnění ledvin, jako jsou glomerulonefritidy a pyelonefritidy. Dalším závažným zdrojem erytrocytů v moči může být ruptura malých cév nebo krvácení při nádorech či poranění ledvin nebo jiných oblastí uropoetického systému, a dále urolitiáza.
- Hemoglobinurie se vyskytuje při intravaskulární hemolýze u hemolytických anemií, při transfúzi inkompatibilní krve nebo paroxysmální hemoglobinurii. Chemicky nelze odlišit hemoglobin v erytrocytech od volného hemoglobinu. To je možné zjistit vyšetřením močového sedimentu, neboť při hemoglobinurii nenalezneme erytrocyty.
Principem chemického zjištění hemoglobinu nebo erytrocytů v moči je tzv. pseudoperoxidázový účinek hemoglobinu. Některé látky, jako např. hemoglobin, hem a jeho deriváty (i chlorofyl), méně též ionty Fe3+, katalyzují neenzymovou oxidaci (dehydrogenaci) vhodných organických sloučenin peroxidem vodíku:
Výhodné je ke sledování reakce použít chromogenní substrát, tj. látku poskytující dehydrogenací výrazně zbarvený produkt (zde aminofenazon, často též benzidin nebo jeho nekancerogenní deriváty). Diagnostické proužky hemoPHAN obsahují v indikační zóně o-tolidin (3,3'-dimethylbenzidin) a kumenhydroperoxid v kysele pufrované směsi. Stejnou reakci katalyzují enzymy – peroxidázy, které slouží k odstraňování peroxidu vodíku vznikajícího v průběhu některých oxidoredukčních dějů v buňkách. Z poznaných krevních elementů mají vysokou peroxidázovou aktivitu leukocyty. Katalytická aktivita enzymu se ztrácí jeho tepelnou denaturací. Pozitivita zkoušky na pseudoperoxidázový účinek hemoglobinu v moči může tedy být způsobena i peroxidázami leukocytů nebo některých bakterií. V tomto případě opakování zkoušky s povařeným vzorkem dá negativní výsledek, zatímco pseudoperoxidázová aktivita neenzymových katalyzátorů zůstává i po povaření vzorku zachována.
Úkol: Průkaz krve a krevního barviva v moči - pdf
Hemoglobin ve stolici- okultní krvácení[upravit | editovat zdroj]
Průkaz okultního (skrytého) krvácení slouží k záchytu časných fází kolorektálního karcinomu, kdy je možná radikální a efektivní léčba. Vyšetření spočívá v zachycení stop krve ve stolici, používají se různé metodické postupy:
- Metody využívají pseudoperoxidázové aktivity hemoglobinu. Pacient musí držet 3 dny před vyšetřením dietu, vyloučit ze stravy nedovařené maso, salámy banány, rajčata, nesmí užívat léky obsahující kyselinu askorbovou nebo acetylsalicylovou. Poté si pacient sám odebírá vzorky ze tří po sobě jdoucích stolic a aplikuje je na testovací karty. Vyhodnocení se provádí v laboratoři, princip je podobný jako u diagnostických proužků hemoPHAN
- Další metody jsou založeny na imunochemickém průkazu hemoglobinu pomocí protilátky proti lidskému hemoglobinu. Imunochemické metody jsou citlivější a specifičtější, není zapotřebí držet před vyšetřením dietu. Pozitivní výsledky musí být ověřeny dalšími diagnostickými metodami.
Úkol: Test na okultní krvácení v zažívacím traktu - pdf
Deriváty hemoglobinu[upravit | editovat zdroj]
K derivátům hemoglobinu se řadí následující typy:
Oxyhemoglobin a deoxyhemoglobin[upravit | editovat zdroj]
Hemoglobin nesoucí kyslík se označuje jako oxyhemoglobin (oxyHb). Po uvolnění kyslíku hovoříme o deoxyhemoglobinu (deoxyHb). V obou formách je železo dvojmocné, neboť pouze hemoglobin obsahující Fe2+ může reverzibilně vázat a přenášet molekulu kyslíku. Oxygenace molekuly hemoglobinu mění elektronový stav komplexu Fe2+ - hem, což se projeví změnou barvy tmavě červeného odstínu typického pro žilní krev na jasně červenou barvu tepenné krve
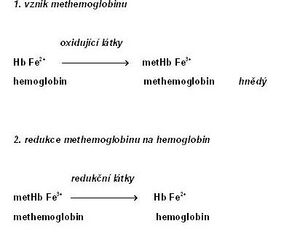
Methemoglobin[upravit | editovat zdroj]
Methemoglobin (metHb) je charakterizován přítomností trojmocného železa, které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík. Na jeho místě váže Methemoglobin (metHb) je charakterizován přítomností trojmocného železa, které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík; na jeho místě váže FeMethemoglobin (metHb) je charakterizován přítomností trojmocného železa, které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík; na jeho místě váže Fe3+ šestou koordinační vazbou molekulu vody. Barva methemoglobinu je čokoládově hnědá. Methemoglobin se stále tvoří v malém množství v erytrocytech. Denní produkce představuje asi 3 %. Jeho zpětná redukce na hemoglobin je zajišťována enzymovými i neenzymovými reakcemi. Enzymovou redukci zabezpečuje NADH-dependentní methemoglobinreduktasa. Neenzymové mechanismy zahrnují působení glutathionu a kyseliny askorbové.
Zvýšená koncentrace methemoglobinu v krvi se označuje jako methemoglobinemie. Příčiny vzniku jsou různé.
- Dědičná methemoglobinemie je obvykle způsobena vrozeným defektem NADH-dependentní methemoglobinreduktasy nebo přítomností abnormálního hemoglobinu M.
- Získaná methemoglobinemie je nejčastější formou methemoglobinemie. Může být vyvolána působením oxidujících látek:
- a) otravou některými látkami (nitrobenzen, anilin a jeho deriváty - např.některá barviva)
- b) působením některých léků (lokální anestetika, fenacetin, sulfonamidy)
- c) zvýšeným obsahem dusičnanů a dusitanů ve vodě a v potravinách
Na zvýšený obsah těchto látek jsou zvláště citliví novorozenci v důsledku nezralosti redukčních systémů a zvýšeného podílu fetálního hemoglobinu, který se snadněji oxiduje. Methemoglobinemie se projevuje cyanózou s charakteristickým šedohnědým odstínem a hypoxií
| Hodnoty methemoglobinu | Příznaky |
|---|---|
| 0 - 2 % | normální hodnota |
| < 10 % | cyanóza |
| < 35 % | cyanóza a další příznaky (bolest hlavy, dušnost) |
| 70 % | smrtelná koncentrace |
Součástí terapie získané methemoglobinemie je podávání některých redukčních činidel – methylénové modři nebo kyseliny askorbové
Karbonylhemoglobin[upravit | editovat zdroj]
Karbonylhemoglobin (COHb) vzniká vazbou oxidu uhelnatého na hemoglobin. Vytvořená vazba je 250 – 300 krát silnější než vazba kyslíku. Karbonylhemoglobin nemůže transportovat kyslík a v důsledku snížené schopnosti krve přenášet kyslík se vyvíjí buněčná hypoxie. V nadbytku kyslíku je vazba oxidu uhelnatého na hemoglobin reverzibilní. Proto je při otravě oxidem uhelnatým nejdůležitější inhalace O22. V malém množství se COHb může vyskytnout i u zdravých osob. U obyvatel měst se prokazují hodnoty kolem 2 %, u silných kuřáků může COHb stoupnout až na 10 % z celkového hemoglobinu. Několikaminutový pobyt v prostředí obsahující 0,1 % CO může zvýšit koncentraci karbonylhemoglobinu na 50 %. Oxid uhelnatý vzniká při nedokonalém spalování fosilních paliv, dále je obsažen ve výfukových plynech a v kouři při požárech v uzavřených místnostech.
| Hodnoty COHb v % | Příznaky |
|---|---|
| 10 | při větší námaze dušnost |
| 20 - 40 | bolesti hlavy, dušnost, únava, zvracení |
| 40 - 60 | hyperventilace, tachykardie, synkopa, křeče |
| 60 - 80 | kóma, smrt |
Karbonylhemoglobin se vyznačuje karmínově červeným zbarvením; také osoby s těžkou otravou oxidem uhelnatým mívají „zdravě“ růžovou barvu pleti. Ve srovnání s hemoglobinem je karbonylhemoglobin odolnější vůči chemickým vlivům, působením různých činidel se mění pomaleji.
Spektrofotometrie derivátů hemoglobinu[upravit | editovat zdroj]
Hemoglobin a jeho deriváty mají ve viditelné oblasti světla charakteristická absorpční spektra, kterých se využívá k jejich analýze a rychlé identifikaci. Pro všechny hemoproteiny jsou typická výrazná absorpční maxima v oblasti 400 - 430 nm, tzv. Soretův pás. Další absorpční vrcholy jsou podstatně nižší. Oxyhemoglobin je charakterizován dvěma neúplně oddělenými maximy v oblasti 540 a 578 nm. Deoxyhemoglobin má jedno absorpční maximum při 555 nm. Hlavní absorpční maximum methemoglobinu je při 630 nm a druhý nevýrazný vrchol při 500 nm je závislý na pH. Reakcí methemoglobinu s kyanidem draselným mizí maximum při 630 nm, neboť vzniká kyanmethemoglobin. Pokles absorbance při 630 nm je úměrný koncentraci methemoglobinu. Kyanmethemoglobin vykazuje široké absorpční maximum při 540 nm, kterého se využívá při stanovení koncentrace hemoglobinu v krvi. Spektrum karbonylhemoglobinu se podobá spektru oxyhemoglobinu, ale poloha vrcholů je posunuta směrem k nižším vlnovým délkám.
| Derivát hemoglobinu | Absorpční maxima (nm) |
|---|---|
| Hemoglobin redukovaný | 431, 555 |
| Oxyhemoglobin | 414, 540, 578 |
| Methemoglobin | 404, 500, 630 |
| Karbonylhemoglobin | 420, 538-540, 568-569 |
| Kyanmethemoglobin | 421, 540 |
Úkol: Spektrofotometrické vyšetření hemoglobinu a jeho derivátů - pdf
Stanovení karbonylhemoglobinu
Stanovení karbonylhemoglobinu v krvi patří mezi základní toxikologická vyšetření. Je objektivním kritériem při hodnocení akutních i chronických otrav oxidem uhelnatým.
- Spektrofotometrické hodnocení. Karbonylhemoglobin lze stanovit rychle spektrofotometricky na základě odečtení posunu absorpčního maxima ředěné krve od 586 nm. Posun maxima ve spektru je závislý na poměru COHb a O22Hb ve vzorku.
- Reakce s taninem. Orientačně lze karbonylhemoglobin stanovit reakcí s taninem nebo Ajatinem (asi od 10 % COHb). Tanin vytváří v přítomnosti karbonylhemoglobinu jahodově červenou sraženinu. V nepřítomnosti karbonylhemoglobinu je zbarvení sraženiny hnědošedé.
- Analyzátory acidobazické rovnováhy. Analýzu toxikologicky nejdůležitějších derivátů hemoglobinu COHb a metHb umožňují rovněž moderní analyzátory acidobazické rovnováhy, které mají zabudovaný fotometrický systém pro jejich měření.
Úkol: Orientační stanovení karbonylhemoglobinu - pdf
Glykovaný hemoglobin HBA1[upravit | editovat zdroj]
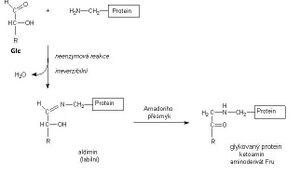
Glykovaný hemoglobin vzniká neenzymovou reakcí mezi hemoglobinem a glukosou v krvi. Jeho tvorba je ireverzibilní.
Hladina glykovaného hemoglobinu proto odráží koncentraci glukosy v krvi po celou dobu existence erytrocytu, tj. asi 120 dní, a využívá se k posouzení úspěšnosti léčby/kompenzace diabetu v období 4–8 týdnů před vyšetřením. Nejčastěji se stanovuje forma stabilní frakce HBA1c. Používá se následující terminologie:
- Glykovaný hemoglobin - suma sacharidových aduktů na N-terminálním konci nebo ε aminoskupinách lysinu v hemoglobinu.
- HbA1 – suma různých minoritních frakcí hemoglobinu (glykovaných), včetně HbA1c, HbA1a1/a2, HbA1b1/b2/b3, HbA1d1/d2/d3 a HbA1e.
- HbA1c – glukosový adukt valinu na N-terminálním konci β-globinu; odpovídá tzv. stabilnímu ketoaminu (N-[1-deoxyfruktosyl]hemoglobinu).
Glykovaný hemoglobin je možné stanovit pomocí iontoměničové chromatografie s následnou spektrofotometrií.
- Hodnocení: Množství glykovaného hemoglobinu se vyjadřuje v % k celkovému hemoglobinu. Referenční meze zdravých dospělých je 2,8–4,0 %.
Úkol: Stanovení glykovaného hemoglobinu - pdf
Železo[upravit | editovat zdroj]
Železo je jedním z nejdůležitějších prvků v lidském organismu. V normálním lidském těle dospělého člověka je obsaženo více než 70 mmol (4,0 - 4,5 g) železa. Největší podíl železa je zabudován v hemoglobinu.
| Forma a funkce | Protein | Množství v g |
|---|---|---|
| AKTIVNÍ ŽELEZO | ||
| Transport kyslíku | hemoglobin | 2,5-3,0 |
| myoglobin | 0,3 | |
| Přenos elektronů | cytochromy, cytochromoxidasa | 0,2 |
| Rozklad peroxidu vodíku | katalasa, peroxidasa | |
| ZÁSOBNÍ ŽELEZO | feritin, hemosiderin | 0,8-1,0 |
| TRANSPORTNÍ ŽELEZO | transferin | 0,003 |
Metabolismus železa[upravit | editovat zdroj]
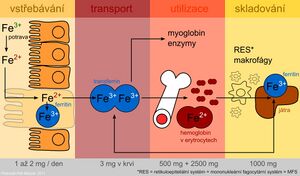
Přítomnost železa je nezbytná pro funkci buněk. Jako součást hemu se účastní transportu kyslíku a jako součást cytochromů podmiňuje přenos elektronů v dýchacím řetězci. Nežádoucím účinkem železa jako přechodného a velmi reaktivního prvku je účast v radikálových reakcích, při nichž vznikají tzv. reaktivní formy kyslíku. Ty mohou poškozovat buněčné membrány, proteiny a DNA. Železo je absorbováno jako Fe2+ aktivním transportem v duodenu a v horní části jejuna. Po vychytání střevní mukózou je část inkorporována do zásobní formy - feritinu v intestinálních buňkách. Část absorbovaného železa přestupuje do plazmy, kde je transportováno ve vazbě na transferin . Plazmatické železo je zachycováno buňkami cílových tkání prostřednictvím receptoru pro transferin a buď je zabudováno do hemu nebo uloženo do zásoby ve formě feritinu. Využití specifické transportní bílkoviny transferinu a zásobního proteinu feritinu pro uskladnění železa představuje ochranné mechanismy, které mají zamezit toxickému působení oxidoredukčně aktivního železa.
Vyšetření metabolismu železa[upravit | editovat zdroj]
V praxi se běžně setkáváme s onemocněními spojenými se změnami metabolismu a utilizace železa. Laboratorní vyšetření metabolismu železa zahrnuje následující vyšetření:
- železo v séru
- sérový transferin a vazebná kapacita pro železo
- sérový feritin
- transferinový receptor
Uvedené parametry jsou důležitými diagnostickými ukazateli pro průkaz poklesu či nárůstu zásob železa ještě ve stádiích, která nejsou doprovázena výraznými klinickými projevy.
Stanovení železa v séru[upravit | editovat zdroj]
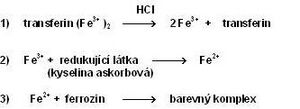
Pro stanovení železa v séru se používají kolorimetrické metody, atomová absorpční spektrofotometrie a další speciální techniky. Nejužívanější jsou fotometrické metody, založené na reakci železa s komplexotvornou látkou. Všechny postupy zahrnují následující kroky:
- uvolnění Fe3+ z vazby na transferin pomocí kyselin nebo tenzidů (např. HCl)
- redukce Fe3+ na Fe2+, která je nezbytná pro reakci s komplexotvorným činidlem, k redukci se používá např. kyselina askorbová
- reakce Fe2+ s komplexotvorným činidlem obsahujícím reaktivní skupiny -N=C-C=N- za vzniku barevného komplexu. Ionty kovu vytvářejí cheláty s dvěma atomy dusíku. V současnosti se využívají především dvě komplexotvorné látky - bathofenentrolin a ferrozin (3-(2-pyridyl)-5,6-bis(4-sulfofenyl)-1,2,4-triazin – PST, chráněný název FerroZine), který má vyšší absorpční koeficient a je lépe rozpustný ve vodě. Hodnocení: Koncentrace sérového železa podléhají cirkadiálnímu rytmu a jsou ovlivněny i dalšími faktory. To omezuje diagnostický význam tohoto parametru. Je špatným ukazatelem tkáňových zásob železa a je nutné ho vždy posuzovat v kombinaci se sérovým transferinem a vazebnou kapacitou pro železo. Snížené koncentrace doprovázejí nedostatek železa, způsobený např. velkými nebo opakovanými krevními ztrátami, nedostatečným příjmem železa potravou nebo narušenou absorpcí. Nález není specifický, neboť se sníženými hladinami se setkáváme rovněž u akutní infekce nebo chronických zánětlivých onemocnění (přesun železa do tkání). Vysoké hladiny železa se vyskytují u hemochromatózy (viz níže), za podmínek předávkování nebo intoxikace železem, při zvýšeném rozpadu erytrocytů a u některých jaterních onemocnění.
Referenční hodnoty: muži: 9-29 μmol/l ženy: 7-28 μmol/l
Úkol: Stanovení Fe v séru kolorimetrickou metodou - pdf
Sérový transferin a vazebná kapacita pro železo[upravit | editovat zdroj]
Železo je transportováno krví ve vazbě na specifický protein s β1-elektroforetickou pohyblivostí – transferin, který je syntetizován v játrech. Rychlost jeho tvorby je nepřímo úměrná zásobám železa v organismu; zvyšuje se při nedostatku železa a při nadbytku klesá. Biologická funkce transferinu spočívá ve schopnosti snadno tvořit netoxické komplexy se železem a přenášet Fe absorbované sliznicí tenkého střeva do kostní dřeně nebo do zásobních forem (feritinu nebo hemosiderinu). Každá molekula transferinu váže 2 atomy Fe3+ (1 g transferinu váže 25,2 μmol železa). Transferin může být stanoven přímo pomocí imunochemických metod nebo nepřímo jako schopnost transferinu vázat železo - tzv. vazebná kapacita pro železo. Celková vazebná kapacita pro železo (TIBC – total iron binding capacity) je množství železa, které je transferin schopen vázat v případě, že všechna vazebná místa jsou obsazena. Odpovídá normální koncentraci transferinu. Obvykle je železem nasycena pouze 1/3 transferinu - vázaná kapacita. Volný transferin bez navázaného železa představuje volnou vazebnou kapacitu (2/3 transferinu), která je k dispozici pro transport železa při zvýšených požadavcích.
Přepočet mezi koncentrací transferinu a celkovou vazebnou kapacitou:
Referenční rozmezí pro koncentraci transferinu v séru (S-transferin) je 2,0-3,6 g/l a pro celkovou vazebnou kapacitu je 50-70μmol/l.
Saturace transferinu: Z hodnot koncentrace železa a transferinu můžeme vypočítat saturaci transferinu (TfS), která je definována jako poměr sérové koncentrace železa k sérové koncentraci transferinu. Jedná se o citlivý parametr pro odhalení latentního nedostatku železa.
Hodnoty saturace transferinu:
- fyziologické hodnoty: 25-50%
- snížení saturace při nedostatku železa: < 15% (nutno zahájit substituční léčbu)
- zvýšení saturace při nadbytku železa: > 50%
Feritin a hemosiderin[upravit | editovat zdroj]
Feritin je nejdůležitější zásobní protein pro železo. Molekula feritinu je přizpůsobena vázat velké množství Fe3+ v rozpustné a netoxické formě pro organismus. Feritin je tvořen vnějším proteinovým obalem z 24 podjednotek – apoferitinem (Mr 440 000), ohraničujícím dutinu, ve které může být soustředěno až 4500 atomů železa ve formě oxyhydroxidu železitého (FeO.OH)n v mikrokrystalické podobě s fosfáty (FeO.OPO3H2). Vstup a výstup atomů železa umožňují póry mezi jednotlivými podjednotkami obalu molekuly feritinu. Normálně je jeho kapacita využita asi z 20 %. Ukládá se do buněk v játrech, slezině a střevní sliznici. V krevním séru se feritin nachází ve velmi nízké koncentraci. Sérové koncentrace feritinu jsou měřítkem zásob železa v organismu. Nízké koncentrace indikují vyčerpání celkové tělesné rezervy železa a slouží k časnému odhalení anemie z nedostatku železa ještě v prelatentní fázi. Zvýšené koncentrace feritinu jsou doprovodným jevem vysokých tkáňových zásob železa. Dále se s nimi setkáváme u mnohých pacientů s onemocněním jater, některými maligními nádory (nádorový marker) nebo zánětlivými onemocněními (pozitivní reaktant akutní fáze).
Referenční rozmezí pro koncentraci feritinu v séru (S-feritin) je pro muže 30-300 μg/l a pro ženy 20-120 μg/l.
Hemosiderin je dalším zásobním proteinem pro železo. Vzniká agregací denaturovaného feritinu s dalšími komponentami. Vytváří partikule o velikosti 1 až 2 μm, které jsou při použití barvení na železo viditelné ve světelném mikroskopu. Hemosiderin obsahuje větší množství Fe než feritin, ale vzhledem ke špatné rozpustnosti ve vodě je obtížně dostupné. Tvoří se za situace, kdy množství železa v organismu převýší skladovací kapacitu feritinu.
Transferinový receptor[upravit | editovat zdroj]
Železo transportované krví transferinem je zachycováno buňkami prostřednictvím specifického transferinového receptoru (TfR). V určitém stádiu vývoje se nachází na povrchu všech buněk, nejvíce je však exprimován na povrchu prekursorů buněk červené řady v kostní dřeni. TfR je transmembránový protein, který je tvořen dvěma identickými podjednotkami, spojenými disulfidovou vazbou. Oddělením extracelulárních domén receptoru se do cirkulace uvolňuje tzv. solubilní (rozpustná) frakce transferinového receptoru (sTfR), který může být v podobě dimeru nebo monomeru. Buňky reagují na snížení zásob železa syntézou zvýšeného množství transferinových receptorů. Zvýšení sTfR je spolehlivým ukazatelem nedostatku železa pro krvetvorbu. Se zvýšenými hladinami sTfR se setkáváme u anemií z nedostatku železa nebo u hemolytických anemií. Cenné je stanovení sTfR u anemických pacientů, u nichž je zvýšen feritin z důvodů reakce akutní fáze. Stanovení koncentrace sTfR je možno využít i u pacientů s transplantovanou kostní dření pro sledování průběhu erytropoézy.
Ke stanovení se používají imunochemické metody.
Poruchy metabolismu železa[upravit | editovat zdroj]
Nedostatek železa (sideropenie)[upravit | editovat zdroj]
Nedostatek železa v organismu bývá zpravidla způsoben jeho nedostatečným vstřebáváním ze střeva nebo chronickými ztrátami krve. Může vyústit v ′′′sideropenickou anemii (hypochromní mikrocytární anemie)′′′, která patří mezi ′′′nejčastější hematologická onemocnění′′′. Anemie je však zpravidla pozdní příznak postupně se vyvíjející sideropenie. V krevním obraze se projeví až po téměř úplném vymizení železa. Proto je potřebné odhalit nedostatek železa v časném stádiu, které ještě není doprovázeno anemií.
Na základě stanovení základních parametrů metabolismu železa rozlišujeme tři stupně nedostatku:
- Prelatentní nedostatek železa je označení pro stav, kdy dochází k postupnému poklesu zásob, ale ještě není ovlivněna dodávka železa do erytroblastů kostní dřeně. Asi u poloviny nemocných jsou hladiny feritinu v séru snížené pod 12 μg/l.
- Při latentním nedostatku železa jsou jeho zásoby v podstatě vyčerpány. Feritin je snížen pod dolní hranici normy a je v tomto stádiu již doprovázen i snížením hladiny železa v séru a sníženou dodávkou do erytroblastů kostní dřeně. Zvyšuje se vazebná kapacita pro železo. Citlivým ukazatelem latentního nedostatku železa je pokles saturace transferinu pod 15 %. Nerozvíjí se však ještě anemie.
- Při manifestním nedostatku železa dochází k rozvoji anemie s poklesem hodnot hemoglobinu pod dolní hranici normy. U anemie z nedostatku železa je typický nález nízkého sérového železa a feritinu, je zvýšená koncentrace transferinu (vazebná kapacita pro železo). U hemolytických anemií nebo při nadbytku železa je naopak sérové železo zvýšené, současně je snížená celková vazebná kapacita pro železo.
| Prelatentní nedostatek železa | Latentní nedostatek železa | Manifestní nedostatek železa |
|---|---|---|
| snižování zásobního železa - pokles feritinu | nedostatek zásobního železa - pokles feritinu | nedostatek zásobního železa - pokles feritinu |
| snížení sérového železa | snížení sérového železa | |
| pokles saturace transferinu pod 15% | pokles transferinu pod 10% | |
| zvýšení celkové vazebné kapacity pro železo | zvýšení celkové vazebné kapacity pro železo | |
| zvýšení sTfR | zvýšení sTfR | |
| snížení koncentrace hemoglobinu - anemie |
Nadbytek železa[upravit | editovat zdroj]
Organismus není vybaven exkreční cestou pro železo, a proto se za určitých okolností může přebytečné železo hromadit ve tkáních. Včasná diagnostika může zabránit poškození tkání nadbytkem železa. Přetížení železem se rozvíjí většinou velmi pomalu. Rozlišujeme 3 stádia:
- Ve stádiu prelatentního nadbytku železa se zvyšuje jeho obsah v orgánech, ale bez překročení jejich zásobní kapacity.
- V období latentního stádia přetížení železem je překročena zásobní kapacita buněk, ale ještě není poškozena funkce orgánů, zvyšuje se hladina feritinu i hladina železa v séru a stoupá saturace transferinu nad 55%.
- Ve fázi manifestního nadbytku železa jsou již poškozeny některé orgány
| Prelatentní nadbytek železa | Latentní nadbytek železa | Manifestní nadbytek železa |
|---|---|---|
| zvyšování zásob železa - zvýšení feritinu | zvyšování zásob železa - zvýšení feritinu nad 300 μg/l | zvyšování zásob železa - zvýšení feritinu (při těžkém postižení nad 2000 μg/l |
| zvýšení železa v séru | výrazné zvýšení železa v séru | |
| zvýšení saturace transferinu nad 55% | zvýšení saturace transferinu (při těžkém postižení může převýšit 90%) |
Hemochromatosa
Hromadění železa v tkáních souvisí s onemocněním, které označujeme jako hemochromatóza.
- Primární hemochromatóza je dědičné onemocnění způsobené zvýšenou resorpcí železa ze střeva. Přebytečné železo se ukládá v parenchymatózních orgánech jako jsou játra, srdce, pankreas, nadledviny. V postižených orgánech působí toxicky a narušuje jejich funkci tím, že může katalyzovat chronické reakce vedoucí k tvorbě volných radikálů. Hlavními klinickými projevy jsou hyperpigmentace kůže, hepatosplenomegalie a diabetes mellitus.
- Sekundární hemochromatóza se může vyvinout jako následek např. opakovaných transfúzí, nadbytečného příjmu přípravků obsahujících železo nebo hemolytické anemie. V biochemickém obraze nalézáme zvyšující se hladiny feritinu a železa v séru, stoupá saturace transferinu při jeho současném poklesu.