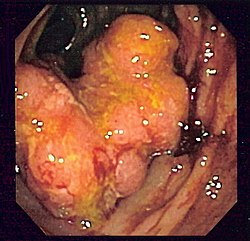
Kolorektální karcinom/terapie
Způsob léčby KR-CA lze určit až po kompletním vyšetření pacienta a stanovení stagingu onemocnění. Každý pacient by měl být zkonzultován na indikačním semináři a výsledná léčba by měla být výsledkem konsenzu onkologa, chirurga, gastroenterologa, popřípadě i patologa. Terapeutický postup se také musí vždy odvíjet od celkového zdravotního stavu pacienta a jeho přání.
Mezi léčebné modality využívané k léčbě KR-CA patří metody endoskopické, chirurgické a onkologické. Zpravidla se nejdříve přistupuje k odstranění nádorové masy, buď endoskopicky nebo častěji chirurgicky, a poté následuje systémová onkologická léčba. Popřípadě u rozsáhlých tumorů předchází chirurgickému řešení ještě neoadjuvantní onkologická terapie.
Mírně se liší postupy terapie u KR-CA lokalizovaného v kolon a v rektu.
Endoskopická léčba[upravit | editovat zdroj]
Nezastupitelný je její význam zejména v diagnostice onemocnění a následné dispenzarizaci pacientů po léčbě. Využívá se zejména ke kurativní léčbě prekanceróz (adenomů) nebo velmi časných stádií KR-CA (carcinoma in situ, pT1), popřípadě k paliativní léčbě ke zprůchodnění stenóz střeva způsobených nádorem (zavedení stentu).
- Kurativní léčba
Dle rozsahu léze užíváme:
- polypektomii (EPE),
- endoskopickou mukozální resekci (EMR),
- endoskopickou submukózní disekci (ESD) – odstranění polypu dohromady i se submukózou.
U pacientů s diagnózou KR-CA pT1 rozhodujeme mezi endoskopickým nebo chirurgickým řešením podle dalších parametrů. U příznivých nádorů dostačuje endoskopická léčba, nicméně u tzv. vysokorizikových pT1 karcinomů přistupujeme k následnému chirurgickému řešení. Kritéria vysokorizikového karcinomu:
- inkompletní odstranění nebo odstranění po částech (ne en block);
- vzdálenost od resekčních okrajů 1 mm a menší;
- nízká diferenciace;
- průkaz invaze do lymfatických cév v histologickém preparátu.
U těchto nemocných provádíme chirurgickou resekci s radikální lymfadenektomií stejně jako u pokročilejších stádií KR-CA.
- Paliativní léčba
Aplikace metalického stentu se využívá buď u akutních střevních obstrukcí k přečkání doby do operačního řešení, popřípadě u inoperabilních a generalizovaných karcinomů v posledních stádiích ke zlepšení kvality života pacienta. Podle různých studií je ale prospěšnost těchto postupů poněkud sporná. Měla by se využívat pouze u pečlivě indikovaných případů po mezioborové konzultaci. U pacientů indikovaných k biologické léčbě bevacizumabem je prokázáno vyšší riziko perforací. [1]
Chirurgická léčba[upravit | editovat zdroj]
Stále jedinou kurativní léčbou kolorektálního karcinomu je onkoradikální resekce (s výjimkou velmi časných stádií řešitelných endoskopicky, viz předchozí odstavec). Indikuje se vždy, když je možné provést kurativní radikální (R0) resekci, tedy odstranit celou nádorovou masu. Popřípadě i z paliativních důvodů, obdobně jako u endoskopické léčby, ke zprůchodnění střevního lumen a tím k prodloužení a zlepšení kvality života pacienta.
- Resekce tračníku
U karcinomu kolon využíváme radikální resekci postiženého úseku střeva společně s odstraněním závěsu (mesocolon). Výhodou tohoto postupu je odstranění většího množství lymfatických uzlin (alespoň 12), odstranění i potenciálně nádorem poškozené tkáně a s omezením pooperačního nádorového rozsevu. Radikalitu dodržujeme i u časnějších stádií (T1, T2). Pokud se nádor nepříznivě nachází v povodí dvou zásobujících tepen, přistupujeme ještě k radikálnějším výkonů – rozšířená resekce, případně subtotální kolektomie (odstranění celého tlustého střeva, s ponecháním rekta a založením ileorektální anastomózy). Vzdálenost na aborálním konci by měla být minimálně 5 cm od tumoru. Pro rozsah resekce je určující rozsah disekce lymfatických uzlin (a cév) podél arteriálního zásobení, kdy dochází k podvazu v blízkosti odstupu kmenů tepen (vysoká ligatura):
- pravá hemikolektomie – ligatura a. ileocolica, a. colica dextra a ramus dexter arteriae colicae mediae (nádor vzestupného tračníku);
- rozšířená pravá hemikolektomie – ligatura a. ileocolica, a. colica dextra a navíc ještě a. colica media (pro tumory ve flexura coli dextra);
- levá hemikolektomie – ligatura a. colica sinistra (nádor sestupného tračníku);
- rozšířená levá hemikolektomie – ligatura a. colica sinistra a a. colica media (nádor při flexura coli sinistra);
- resekce sigmatu – ligatury a. mesenterica inferior.[2]
Laparoskopický přístup je využívanou alternativou ke klasickému postupu, zejména pak u nádorů levostranného kolon. [1]
- Resekce rekta
Nejpoužívanější postup je totální mezorektální excize (TME), která významně omezuje výskyt lokálních recidiv. Prognostickým faktorem pro úspěšnost TME je hlavně pozitivita resekčních okrajů. V dnešní době užíváme moderní miniinvazivní, robotické a laparoskopické metody, které jsou však stále dostatečně radikální, zároveň ale pro pacienta méně mutilující. Chirurgické výkony lze rozdělit na:
- Kurativní výkony (potenciálně):
- standardní operace – resekce rekta (+ mesorekta), může být s amputací sfinkteru, ale i sfinkter zachovávající (i ta je dostatečně onkoradikální);
- extenzivní operace – resekce rekta, mesorekta a abdominopelvických lymfatických uzlin a cév;
- ultraextenzivní operace – navíc s resekcí vnitřních iliackých cév.[2]
- Paliativní výkony spočívají v:
- odstranění nádoru – ve většině případů je lepší nádor odstranit, i když je pro staging onemocnění nebo celkový stav pacienta vyloučena kurativní resekce, každý rostoucí nádor pacienta ohrožuje vznikem ilea, perforací stěny střevní, rozpadem nádoru (nekróza);
- řešení překážky v pasáži střeva (tou je nádor) – stomií nebo bypassem;
- léčbě bolesti.
- Resekce jaterních metastáz
Játra jsou orgánem, kde nejčastěji nalézáme metastázy KR-CA a jejich léčba úzce souvisí s prognózou pacienta.
- Standardní předoperační vyšetření [3]
- Kolonoskopie s biopsií – pokud není možné tak dvojkontrastní irigografie,
- sonografie jater
- CT jater – při nejasném nálezu nebo nálezu jaterních metastáz na sono,
- CT malé pánve,
- RTG plic
- CT plic – při nálezu metastáz na RTG
- bronchoskopie – při podezření na metastázy, k vyloučení duplicity,
- urologické vyšetření – při hematurii nebo urologických potížích s podezřením na progresi onemocnění,
- gynekologické vyšetření,
- stanovení onkomarkerů – CEA, CA 19–9,
- u karcinomu rekta: transrektální sonografie, anorektální manometrie.
Onkologická léčba[upravit | editovat zdroj]
Téměř každý pacient s KR-CA podstupuje onkologickou léčbu v nějaké z jejích podob – radioterapie, chemoterapie, biologická léčba. Dle léčebné sekvence rozlišujeme neoadjuvantní, adjuvantní a samostatnou onkologickou léčbu. Radioterapie má využití zejména u karcinomu rekta, neboť je k ní vysoce senzitivní a navíc má velkou náchylnost k lokoregionálnímu šíření (karcinom kolon zakládá spíše vzdálené metastázy), aplikujeme dávku 30 Gy. [4]
- Neoadjuvantní léčba
Neoadjuvantní léčbu využíváme zejména u karcinomu rekta – buď radioterapii samostatně nebo v kombinaci s chemoterapií (tj. chemoradioterapii). U rozsáhlých tumorů (T3–T4, N+) při neoadjuvantní (předoperační) léčbě dochází ke zmenšení nádorové masy (tzv. downstaging), a tím k lepší operabilitě nálezu (vyšší procento sfinkter zachovávající operací), zvýšení procenta kurativních resekcí a nižšímu výskytu lokálních recidiv. Nicméně nebylo potvrzeno celkově delší přežití pacientů podstupujících neoadjuvantní terapii. [1] Kombinace chemo- a radioterapie je provázená poněkud vyšší toxicitou. Obecně musíme indikaci neoadjuvantní terapie zvažovat vzhledem ke stavu pacienta, aby významně nezhoršovala kvalitu jeho života. Chemoterapeutikem volby je 5-fluoruracil (5-FU), alternativou pak kapecitabin (p.o.), případně v kombinaci s oxaliplatinou či irinotekanem. [5]Především v kombinacích jako FOLFOX (leukovorin, 5-FU, oxaliplatina).
Leukovorin je biomodulátor a přidává se z důvodu zvýšení účinku 5-FU a snížení toxicity.
- Adjuvantní léčba
Pokud je to po chirurgické léčbě nutné, přichází na řadu systémová léčba, jejímž cílem je odstranit případné mikrometastázy, zabránit dalšímu šíření onemocnění nebo případnému relapsu. O zahájení adjuvantní léčby se rozhodujeme znovu podle stavu pacienta a vlastností nádoru. Obecně se doporučuje zejména u stádia III, kde zvyšuje dlouhodobé přežití bez známek onemocnění až o 30 % a u nádorů stadia II s vysokým rizikem recidivy. [1] Adjuvantní chemoterapie zlepšuje výsledky 5letého přežití o 10 %. [3]
- Samostatná onkologická léčba
Paliativní samostatnou onkologickou léčbu užíváme u pacientů s inoperabilním pokročilým nálezem, prodlužujeme jednak medián progrese onemocnění a také medián přežití. [1]
- Cílená léčba
Novinkou v léčbě KR-CA v posledních 10 letech je zavedení cílené léčby, někdy také označované jako biologická léčba. V aplikaci spolu s chemoterapií zvyšuje její účinnost (zvýšení léčebné odpovědi a prodloužení mediánu přežití pacientů). Principem cílené léčby je ovlivňování konkrétních signálních drah nutných k růstu nádoru. V ČR se nyní k cílené léčbě využívají tři léčiva: bevacizumab (protilátka proti vaskulárnímu endoteliálnímu růstovému faktoru A – VEGF-A), cetuximab a panitumumab (inhibitory receptoru pro epidermální růstový faktor – EGFR). [6]
Shrnutí[upravit | editovat zdroj]
Obecné rizikové faktory:
- méně než 12 resekovaných lymfatických uzlin;
- nízký stupeň diferenciace nádoru (grade 3 a 4);
- prorůstání nádoru celou stěnou střeva (T4);
- perforace nebo obstrukce střeva jako primární projev nádoru;
- angioinvazie, lymfangioinvaze nebo perineurální invaze;
- neznámé resekční okraje;
- zvýšená hladina karcinoembryonálního antigenu (CEA);
- mucinózní složka nádoru.
Strategie léčby dle stagingu onemocnění v době diagnózy: [7]
| St. I | chirurgická léčba |
| St. II | chirurgická léčba (v případě N1 NX následuje chemoterapie) |
| St. III | operace a vždy chemoterapie |
| St. IV | resekce, nebo indukční terapie a pak resekce, nebo paliativní léčba |
Odkazy[upravit | editovat zdroj]
Související články[upravit | editovat zdroj]
Externí odkazy[upravit | editovat zdroj]
Reference[upravit | editovat zdroj]
- ↑ a b c d e ZAVORAL, Miroslav, et al. Terapie kolorektálního karcinomu [online]. Zdraví E15, ©2012. Poslední revize 6.4.2012, [cit. 2015-12-02]. <https://web.archive.org/web/20160331222721/http://zdravi.e15.cz/clanek/postgradualni-medicina/terapie-kolorektalniho-karcinomu-464247>.
- ↑ a b ŠIMŠA, Jaromír. Onkochirurgie [přednáška k předmětu Chirurgie-předstátnicová stáž, obor Chirurgie, 1. LF UK Univerzita Karlova v Praze]. Praha. 2011-10-08.
- ↑ a b Česká gastroenterologická společnost ČLS JEP. Kolorektální karcinom - diagnostika a léčba [online]. [cit. 2015-11-13]. <http://www.cls.cz/seznam-doporucenych-postupu>.
- ↑ LIPSKÁ, Ludmila a Vladimír VISOKAI. Recidiva kolorektálního karcinomu: komplexní přístup z pohledu chirurga. 1. vyd. Praha: Grada, 2009, 431 s.
- ↑ LIPSKÁ, Ludmila a Vladimír VISOKAI. Recidiva kolorektálního karcinomu: komplexní přístup z pohledu chirurga. 1. vyd. Praha: Grada, 2009, 431 s.
- ↑ [online]. [cit. 2016-1-17]. Dostupné z: https://web.archive.org/web/20160331222721/http://zdravi.e15.cz/clanek/postgradualni-medicina/biologicka-lecba-kolorektalniho-karcinomu-466755.
- ↑ ŠMAKAL, Martin. Komplexní léčení nádorů - role onkologa [přednáška k předmětu Chirurgie - předstátnicová stáž, obor Chirurgie, 1. LF UK Univerzita Karlova v Praze]. Praha. 2011-10-21.
Použitá literatura[upravit | editovat zdroj]
- ZAVORAL, Miroslav, et al. Terapie kolorektálního karcinomu [online]. Zdraví E15, ©2012. Poslední revize 6.4.2012, [cit. 2015-12-02]. <https://web.archive.org/web/20160331222721/http://zdravi.e15.cz/clanek/postgradualni-medicina/terapie-kolorektalniho-karcinomu-464247>.
Doporučená literatura[upravit | editovat zdroj]
- ČEŠKA, Richard a Tomáš ŠTULC, et al. Interna. 2. vydání. TRITON, 2022. 870 s. ISBN 978-80-7387-885-6.
- KRŠKA, Zdeněk a David HOSKOVEC, et al. Chirurgická onkologie. 1. vydání. Praha : Grada, 2014. 904 s. ISBN 978-80-247-4284-7.