Methemoglobin: Porovnání verzí
m (typo, názv, kat) |
m (vložený článek) |
||
| Řádek 1: | Řádek 1: | ||
<!---------------------------------------------------------------------------------------------------------------- | |||
* VLOŽENÝ ČLÁNEK | |||
* Pozor - tento článek je využíván dalšími články, do kterých je vložen. Buďte prosím opatrní při jeho editaci: | |||
* 1. Nemažte příkazy <noinclude> </noinclude>. Označují části článku, které se při vkládání nepřenášejí. | |||
* 2. Neměňte úrovně použitých nadpisů. Neuvážené použití nadpisů vyšší úrovně by mohlo znepřehlednit jiné články. | |||
* 3. Rozsáhlejší editace, rozšíření či zkrácení článku by mohly narušit koncept dalších článků. Změny projednejte v diskusi. | |||
* Seznam článků, do kterých je tento článek vložen, naleznete v seznamu odkazujících článků pod odkazem "Odkazuje sem". | |||
* | |||
* Neodstraňujte, prosím, tento komentář. V případě nejasností kontaktujte redakci (redakce@wikiskripta.eu) | |||
* | |||
* Toto upozornění se vkládá šablonou {{subst:Vložený článek}} | |||
-------------------------------------------------------------------------------------------------------------->[[Kategorie:Vložené články]] | |||
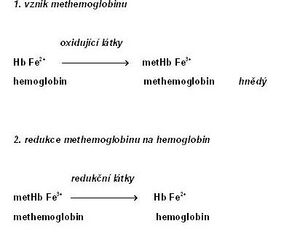
'''Methemoglobin''' (metHb) je charakterizován přítomností '''trojmocného železa''', které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík. Na jeho místě váže Fe<sup>3+</sup> šestou koordinační vazbou molekulu vody. Barva methemoglobinu je čokoládově hnědá. | '''Methemoglobin''' (metHb) je charakterizován přítomností '''trojmocného železa''', které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík. Na jeho místě váže Fe<sup>3+</sup> šestou koordinační vazbou molekulu vody. Barva methemoglobinu je čokoládově hnědá. | ||
Verze z 6. 5. 2010, 06:56
Methemoglobin (metHb) je charakterizován přítomností trojmocného železa, které vzniká oxidací dvojmocného železa v hemoglobinu. Methemoglobin ztrácí schopnost reverzibilně vázat kyslík. Na jeho místě váže Fe3+ šestou koordinační vazbou molekulu vody. Barva methemoglobinu je čokoládově hnědá.
Methemoglobin se stále tvoří v malém množství v erytrocytech. Denní produkce představuje asi 3 %. Jeho zpětná redukce na hemoglobin je zajišťována enzymovými i neenzymovými reakcemi. Enzymovou redukci zabezpečuje NADH-dependentní methemoglobinreduktáza. Neenzymové mechanismy zahrnují působení glutathionu a kyseliny askorbové.
Zvýšená koncentrace methemoglobinu v krvi se označuje jako methemoglobinemie. Příčiny vzniku jsou různé.
- Dědičná methemoglobinemie je obvykle způsobena vrozeným defektem NADH-dependentní methemoglobinreduktasy nebo přítomností abnormálního hemoglobinu M.
- Získaná methemoglobinemie je nejčastější formou methemoglobinemie. Může být vyvolána působením oxidujících látek:
- otravou některými látkami (nitrobenzen, anilin a jeho deriváty - např. některá barviva)
- působením některých léků (lokální anestetika, fenacetin, sulfonamidy)
- zvýšeným obsahem dusičnanů a dusitanů ve vodě a v potravinách.
Na zvýšený obsah těchto látek jsou zvláště citliví novorozenci v důsledku nezralosti redukčních systémů a zvýšeného podílu fetálního hemoglobinu, který se snadněji oxiduje. Methemoglobinemie se projevuje cyanózou s charakteristickým šedohnědým odstínem a hypoxií.
| Hodnoty methemoglobinu | Příznaky |
|---|---|
| 0–2 % | normální hodnota |
| < 10 % | cyanóza |
| < 35 % | cyanóza a další příznaky (bolest hlavy, dušnost) |
| 70 % | smrtelná koncentrace |
Součástí terapie získané methemoglobinemie je podávání některých redukčních činidel – methylénové modři nebo kyseliny askorbové.