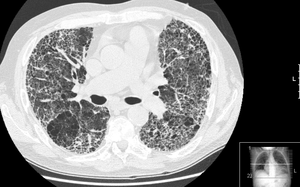
Intersticiální plicní procesy
(přesměrováno z Plicní fibróza)
Intersticiální plicní procesy (IPP, též fibrotizující plicní procesy) jsou imunopatologické procesy na úrovni intersticia plic, tj. v oblasti interalveolární, v alveolech a v peribronchiu. Zabraňují účinné výměně plynů na alveolo-kapilární membráně a vedou k respirační insuficienci.[1]
Jedná se o skupinu chorob různé etiologie, pro které je typická různá míra zánětlivého a/nebo fibrotického postižení plicního parenchymu. Postižení plic se obvykle projevuje námahovou dušností, váhovým úbytkem, subfebriliemi a četnějšími respiračními infekty. V pozdních stadiích se rozvíjí cor pulmonale se známkami pravostranné srdeční dekompenzace.[2]
Plicní fibrózy obecně
Klasifikace
- Difuzní plicní procesy ze známých příčin: exogenní alergické alveolitidy (EAA), pneumokoniózy, postradiační pneumonie, polékové poškození plic (např. u amiodaronu a metotrexátu);
- Idiopatické intersticiální pneumonie: idiopatická plicní fibróza (IPF); nespecifická intersticiální pneumonitida; lymfocytární intersticiální pneumonitida; deskvamativní intersticiální pneumonitida; intersticiální plicní nemoc sdružená s respirační bronchiolitidou; kryptogenní organizující pneumonie; akutní intersticiální pneumonitida;
- Granulomatózy − sarkoidóza, plicní histiocytóza z Langerhansových buněk, granulomatóza s polyangiitidou aj. vaskulitidy atd.;
- Jiné: eozinofilní pneumonie, lymfangioleiomyomatóza, alveolární proteinóza atd.[2][1]
Patogeneze
V patogenezi hraje roli ukládání fibrinu podél alveolárních stěn → v alveolech se vytvoří tzv. hyalinní membrány. Následuje zánětlivá fáze s infiltrací neutrofily (později makrofágy a lymfocyty), jejichž prostřednictvím reparační procesy vyúsťují ve fibrózu. Dalším patogenetickým dějem je proliferace alveolárních buněk, organizace fibrinózního exsudátu, ukládání kolagenu → reparace / fibróza.[3]
Důsledky intersticiálních nemocí plic
- Hypoxémie (↓ paO2) zejména námahová již v počátečních stádiích s hyperventilací s tendencí k respirační alkalóze (↓ paCO2);
- později klidová hypoxémie (↓ paO2) a hypoventilace;
- plicní hypertenze → cor pulmonale.[3]
Společné rysy
Mezi společné rysy patří námahová a poté i klidová dušnost. IST jsou často provázené dráždivým kašlem. Na skiagramu mohou být patrné retikulonodulace či voštinovitá plíce. V poslechovém nálezu mohou být krepitace.[1]
Vyšetření
V laboratorní diagnostice volíme vyšetření k vyloučení poškození jiných orgánů, základní imunologické vyšetření, vyšetření autoprotilátek. V indikovaných případech v rámci screeningu vyloučení postižení glomerulu, metabolizmus kalcia a sérový angiotenzin konvertující enzym u nemocných se suspekcí na sarkoidózu. Důležité je vyšetření plicních funkcí a parametrů respirace v klidu, event. při zátěži a skiagram hrudníku ve dvou projekcích (negativní nález však nevylučuje IPP!). Dále používáme v diagnostice výpočetní tomografii s vysokou rozlišovací schopností (HRCT) posuzující typ a rozsah postižení plicního parenchymu. Z invazivních vyšetření nám pomůže bronchoskopie s bronchoalveolární laváží a transbronchiální biopsií, event. chirurgická plicní biopsie. [2]
Terapie
Terapii volíme dle etiologie (je-li známa). Prvním krokem je zastavit expozici škodlivým vdechovaným činitelům.
Farmakoterapie
- systémová kortikoterapie v dávkách odpovídajících tíži postižení
- indikace: idiopatická nespecifická intersticiální pneumonitida (NSIP), závažná exogenní alergická alveolitida (EAA), polékové plicní postižení, eosinofilní pneumonie, kryptogenní organizující pneumonie (COP), sarkoidózy s postižením plicních funkcí;
- systémová kortikoterapie v kombinaci s dalšími imunosupresivy (např. metotrexát, azathioprin, cyklofosfamid)
- systémové choroby pojiva, jiné autoimunitní syndromy;
- N-acetylcystein – idiopatická plicní fibróza (IPF),
- inhibitory protonové pumpy – IPF,
- inhalační bronchodilatancia – silikóza, uhlokopská pneumokonióza,
- inhalační kortikosteroidy – sarkoidóza s bronchiální hyperreaktivitou,
- makrolidy – některé formy organizující pneumonie.[2]
Nefarmakologická léčba
- oxygenoterapie,
- balneoterapie,
- fyzioterapie,
- transplantace plic.[2]
Prognóza
Nejvážnější prognózu má idiopatická plicní fibróza (IPF) – transplantace plic, event. léčba pirfenidonem[2] (imunosupresivum – tlumí proliferaci fibroblastů, tvorbu cytokinů a proteinů spojených s fibrózou a zvýšenou biosyntézu a akumulaci extracelulární matrix v reakci na cytokinové růstové faktory).
Idiopatická plicní fibróza (IPF)
Jedná se o difúzní, primárně fibrotizující plicní proces.
Patogeneze
Pravděpodobně se jedná o uniformní patologickou odpověď plicní tkáně na infekční i neinfekční agens. Tato způsobují poškození výstelky alveolů, a tak vyúsťují v progredující a nekontrolovatelné jizvení. Zánětlivá reakce jako taková se může vyskytnout až sekundárně.
Epidemiologie
- Pacienti jsou nejčastěji ve věku mezi 40 a 70 lety.
- Incidence u žen je 7,4/100 000 a u mužů 10,7/100 000.
- Vyskytuje se sporadicky, je stejně rozšířená ve všech lokalitách, familiární případy jsou vzácné.
- Onemocnění je prakticky neléčitelné, i při adekvátní léčbě obvykle přežití nepřesahuje 3–5 let.
Klinický obraz
- Začátek – protrahovaný neproduktivní kašel s v čase se zhoršující námahovou dušností, únava, úbytek na váze, tachypnoe;
- U 2/3 pacientů se vyskytují paličkovité prsty s nehty ve tvaru hodinového sklíčka.
- Obraz CHOPN bez obstrukční vady, v pozdější fázi restrikční poškozeni plic – snížení FVC.
- Přes typicky vleklý postupně se zhoršující průběh se u některých pacientů mohou vyskytnou akutní exacerbace:
- náhlé klinické zhoršení;
- pokles plicních funkcí;
- radiologický obraz tzv. mléčného skla (svědčí pro alveolitidu).
Diagnostika
Zde jsou rozhodující HRCT a typický klinický nález, pokud jsou vyloučeny systémové choroby pojiva a exogenní příčina, není nutná biopsie.
- HRCT obraz plic: plicní fibróza s obrazem voštinaté plíce v bazích plic a minimální okrsky aktivních změn.
- Histologie z plicní biopsie.
- U pacientů neschopných podstoupit chirurgickou biopsii musíme vystačit s RTG obrazem a bronchoskopií.
- RTG: zmnožená plicní kresba až retikulace – voštinovitá plíce.
- Funkční vyšetření: restriktivní ventilační porucha, porucha plicní poddajnosti.
Terapie
- Protizánětlivé a imunosupresivní léky jsou málo účinné, protože hlavním patologickým mechanismem je zde patologická fibroprodukce, dnes se tedy v léčbě nepoužívají.
- Pirfenidon
 – inhibuje fibrózu, indikován u pacientů s FVC 50–80%. Dávkování 3x3cps – celkově 2403 mg.
– inhibuje fibrózu, indikován u pacientů s FVC 50–80%. Dávkování 3x3cps – celkově 2403 mg. - Nintedanib
 – inhibitor tyrozinkinázy na VEGFR, FGFR a PDGFR
– inhibitor tyrozinkinázy na VEGFR, FGFR a PDGFR - Časné alveolární léze: N-acetylcystein 3krát 600 mg (antioxidační působení).
- Akutní exacerbace: vysoké dávky kortikoidů, antikoagulační léčba a antibiotika. Jako prevence exacerbací se podávají PPI (blokátory protonové pumpy).
- Pokročilá onemocnění s hypoxemií: dlouhodobá domácí oxygenoterapie a zvážení transplantace plic.
- Kortikoidy v dlouhodobé terapii jsou neefektivní, protože fibrotizace není navozena zánětlivou reakcí.[5][6][7]
Souhrnné video
Exogenní alergická alveolitida (EAA)
Exogenní alergická alveolitida (nebo též hypersenzitivní pneumonitida, farmářská plíce, holubářská plíce) zahrnuje skupinu imunologicky podmíněných chorob (přecitlivělost III. typu) s granulomatózním zánětem v bronchiolech + alveolech. Jedná se o intersticiální plicní fibrózu podmíněnou opakovaným kontaktem s určitým alergenem. Nejohroženější skupinou jsou pracovníci v rostlinné a živočišné výrobě po opakovaných expozicích plesnivému senu, slámě a zrní. Exogenní alergická alveolitida vzniká i při práci s plesnivým sladem, s kožešinami, plesnivými sýry, s peřím a exkrementy ptáků. U dětí je vzácná, vzniká nejčastěji inhalací organických prachů z ptáků (holubi, papoušci, andulky).
Diagnostika
- Anamnéza, laboratorní známky zánětu, precipitující protilátky (specifické IgG) v séru proti vyvolávajícímu antigenu,
- RTG hrudníku: retikulonodulární kresba se skvrnitými prchavými infiltráty,
- BAL: bývá lymfocytární alveolitida, ↓ CD4/CD8,
- chronická fáze: na RTG + HRCT obraz intersticiální plicní fibrózy / voštinové plíce; restrikce, porucha difúzní kapacity plic, hypoxémie; plicní biopsie.
Klinický obraz
- Akutní
Akutní forma je reverzibilní a rozvíjí se během asi 6 hodin po intenzivní expozici antigenu. Odeznívá do 48 hodin. Fyzikálně je prokazatelný krepitus nad plicními bazemi. Charakteristické jsou tyto projevy:
- Chronická
Pokud expozice antigenu přetrvává, vyvíjí se chronická forma exogenní alergické alveolitidy. Při opakované expozici také stačí nižší koncentrace příslušného antigenu. Dochází k ireverzibilnímu onemocnění intersticiální plicní fibróze (restrikční porucha). Příznaky:
- ztráta na váze, únava, kašel, dušnost a cyanóza, cor pulmonale, paličkovité prsty, nakonec respirační selhání.
Terapie
- Eliminace antigenů – nutné trvalé vyřazení pracovníka z expozice (u nemoci z povolání),
- kortikoidy,
- oxygenoterapie.[8][9][10]
Profesionální pneumokoniózy
Pneumokoniózy jsou skupina profesionálních onemocnění, která vznikají dlouhodobou inhalací vzduchu obsahujícího specifické anorganické částečky. Podkladem plicních změn je reakce imunokompetentních buněk na tyto částečky, která vede k poškození intersticia plic.[11]
Typy onemocnění
- Silikóza,
- azbestóza,
- uhlokopská pneumokonióza,
- berylióza,
- talkóza – vzniká po expozici prachu talku (při jeho těžbě a mletí), možné obrazy onemocnění:
- nodulární léze,
- difuzní intersticiální fibróza,
- granulomatózní reakce okolo cizích těles,
- plicní postižení při inhalaci tvrdých kovů – kobaltová, wolframová, karbidová, možné obrazy onemocnění:
- chronické difúzní inersticiální postižení s obrazem plicní fibrózy,
- akutní a subakutní intersticiální postižení s obrazem EAA nebo BOOP,
- obstrukční plicní postižení připomínající profesionální astma.
V dnešní době se s těmito onemocněními setkáváme spíše zřídka (výskyt klesá vlivem prevence v pracovním prostředí).[11]
Typy změn
Charakter zánětlivých změn závisí na tvaru a velikosti vdechovaných částic, délce a intenzitě expozice. Anorganické částice lze z hlediska tvaru rozdělit na fibrogenní (silikóza, azbestóza) a nefibrogenní (ostatní). Obecně lze říci, že onemocnění vyvolaná fibrogenními částicemi jsou horší, protože nereagují na protizánětlivou léčbu a tím pádem mají sklon k trvalé progresi a jejich prognóza je velmi špatná.[11]
Projevy onemocnění
Postupný pokles plicních funkcí, zhoršující se kašel, dušnost a vznik respirační insuficience.[11]
Diagnostika
- Anamnéza – symptomy (kašel, dušnost), pracovní a sociální anamnéza,
- RTG plic,
- funkční vyšetření plic (spirometrie),
- BAL – pokud potřebujeme průkaz anorganických částic,
- biopsie už se většinou neprovádí.[11]
Terapie
- Prevence vzniku onemocnění (ochranné pomůcky, limity v pracovním prostředí),
- eliminace další expozice,
- terapie nasedajících infekcí,
- dlouhodobá domácí oxygenoterapie (DDOT),
- dechová rehabilitace,
- transplantace plic (v indikovaných případech).[11]
Plicní projevy u systémových chorob pojiva
Systémová onemocnění pojiva jsou autoimunitní onemocnění s multiorgánovým postižením na základě vaskulitidy; častá artritida, postižení svalů + kůže. Vznik fibrotizující alveolitidy je reakcí na imunokomplexy deponované v plicních kapilárách. Léčbou je kortikoterapie.[12]
- Intersticiální postižení u 1,5 až 4,5 %;
- klinicky i histologicky totožné s KFA;
- prognóza: při výskytu plicních změn nepříznivá;
- terapie: glukokortikoidy + imunosupresiva.[12]
- Plicní postižení v 50 až 60 %: nejč. pleuritida, IPP, ojediněle akutní pneumonie;
- RTG: retikulonodulární stíny s max. postižení dolních plicních polí;
- terapie: kortikoidy + penicillamin/cyclophosphamid;
- přežití 10 až 14 let (příčinou úmrtí renální selhání, endarteriitida nebo sek. pneumonie).[12]
- Sklerodermie (progresivní systémová skleróza)
- IPP až u 80 % pac.[12]
Postradiační fibróza plic
Plicní fibróza představuje konečné stadium postradiačních plicních změn.
- Po ozáření plicní tkáně ionizujícím záření v dávkách > 8 Gy za 30 týdnů,
- ionizujícím zářením způsobené nekrotické změny hojeny fibrotickou jizvou,
- klinicky: suchý kašel, zhoršující se dušnost (restrikční porucha se ↓ difúzí),
- dif. dg.: radiační pneumonitida (exsudativní alveolitis z poškození pneumocytů + endotelu),
- th.: u drobných infiltrátů bez léčby, u symptomatických kortikoidy.[13]
Poléková plicní fibróza
Polékovou fibrózou plic nazýváme rozvoj intersticiální pneumonie a fibrózy v rámci přecitlivělosti anebo toxického účinku léku (bleomycin![]() , MTX
, MTX![]() , amiodaron
, amiodaron![]() , nitrofurantoin
, nitrofurantoin![]() [14] inhalace O2 ve vysokých koncentracích):
[14] inhalace O2 ve vysokých koncentracích):
- přecitlivělost: ATB (penicilin, ampicilin, nitrofurantoin), některá cytostatika (MTX),
- přímá toxicita: cytostatika (bleomycin, cyclofosfamid
 ) → cytostatická plíce.
) → cytostatická plíce.
Může se pojevit jako akutní nebo chronický stav.[15]
Klinický obraz
- Dušnost,
- suchý, dráždivý kašel,
- RTG: lokalizované/difúzní postižení intersticia, pozdní formou voštinovité plíce.
Terapie
- Vynechání léku, glukokortikoidy.[15]
Odkazy
Související články
- Idiopatická plicní fibróza • Revmatoidní artritida • Systémový lupus erythematodes • Sklerodermie • Sjögrenův syndrom
- Restrikce dýchání/Repetitorium
Reference
- ↑ a b c HOMOLKA, Jiří, et al. Vnitřní lékařství Svazek III. první vydání. Praha : nakladatelství Galen, 2001. ISBN 80-7262-131-9.
- ↑ a b c d e f ŠTERCLOVÁ, M a M VAŠÁKOVÁ. Intersticiální plicní procesy – proč je potřeba správně stanovit diagnózu?. Interní Med [online]. 2013, roč. 15, vol. 8-9, s. 261-262, dostupné také z <https://www.internimedicina.cz/pdfs/int/2013/08/06.pdf>.
- ↑ a b DÍTĚ, P., et al. Vnitřní lékařství. 2. vydání. Praha : Galén, 2007. ISBN 978-80-7262-496-6.
- ↑ KOLEKTIV, Marek. Farmakoterapie vnitřních nemocí - 4. zcela přepracované a doplněné vydání. - vydání. Grada Publishing a.s., 2010. 777 s. s. 170. ISBN 9788024726397.
- ↑ BENEŠ, Jiří. Studijní materiály [online]. [cit. 2010]. <http://jirben.wz.cz>.
- ↑ ČEŠKA, Richard, et al. Interna. 1. vydání. Praha : Triton, 2010. 855 s. ISBN 978-80-7387-423-0.
- ↑ VAŠÁKOVÁ, Martina. Léčba idiopatické plicní fibrózy. Remedia [online]. 2012, roč. 2012, vol. 2, s. 398-402, dostupné také z <http://www.remedia.cz/Clanky/Farmakoterapie/Lecba-idiopaticke-plicni-fibrozy/6-L-1oN.magarticle.aspx>. ISSN 0862-8947.
- ↑ BENEŠ, Jiří. Studijní materiály [online]. [cit. 11.3.2010]. <http://jirben.wz.cz>.
- ↑ DÍTĚ, P., et al. Vnitřní lékařství. 2. vydání. Praha : Galén, 2007. ISBN 978-80-7262-496-6.
- ↑ TUČEK, Milan, Miroslav CIKRT a Daniela PELCLOVÁ. Pracovní lékařství pro praxi : Příručka s doporučenými standardy. 1. vydání. Praha : Grada Publishing, 2005. s. 69-70. ISBN 80-247-0927-9.
- ↑ a b c d e f ČEŠKA, Richard, et al. Interna. 1. vydání. Praha : Triton, 2010. 855 s. s. 460-465. ISBN 978-80-7387-423-0.
- ↑ a b c d DÍTĚ, P., et al. Vnitřní lékařství. 2. vydání. Praha : Galén, 2007. ISBN 978-80-7262-496-6.
- ↑ DÍTĚ, P., et al. Vnitřní lékařství. 2. vydání. Praha : Galén, 2007. ISBN 978-80-7262-496-6.
- ↑ GOEMAERE, Natascha N T, Karin GRIJM a Peter Th W VAN HAL, et al. Nitrofurantoin-induced pulmonary fibrosis: a case report. J Med Case Rep [online]. 2008, vol. 2, s. 169, dostupné také z <https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2408600/?tool=pubmed>. ISSN 1752-1947.
- ↑ a b DÍTĚ, P., et al. Vnitřní lékařství. 2. vydání. Praha : Galén, 2007. ISBN 978-80-7262-496-6.